
| A. | 滤液中一定含有Zn2+,可能含有Cu2+ | |
| B. | 所得滤渣质量可能等于加入的Zn粉和Cu粉质量 | |
| C. | 如果滤渣中有Zn,则滤液可能为浅绿色 | |
| D. | 如果滤液中含有Ag+,则滤渣一定为纯净物 |
分析 锌比铁活泼,铁铜活泼,铜比银活泼,将一定量的Zn粉和Cu粉加入一定量Fe(NO3)2和AgNO3混合溶液中,锌先和硝酸银反应,后和硝酸亚铁反应,如果锌不足时,铜能和硝酸银反应生成硝酸铜和银.
解答 解:A、滤液中一定含有锌和硝酸银反应生成的Zn2+,如果锌不足以和硝酸银反应,则铜和硝酸银反应生成硝酸铜和银,则滤液中含有Cu2+,该选项说法正确;
B、锌和硝酸银、硝酸亚铁反应的化学方程式及其质量关系为:
Zn+2AgNO3=Zn(NO3)2+2Ag,Zn+Fe(NO3)2=Zn(NO3)2+Fe,
65 216 65 56
由以上质量关系可知,锌和硝酸银反应时固体质量增大,和硝酸亚铁反应时固体质量减小,因此所得滤渣质量可能等于加入的Zn粉和Cu粉质量,该选项说法正确;
C、如果滤渣中有Zn,硝酸银和硝酸亚铁都已经完全反应,则滤液不可能为浅绿色,该选项说法不正确;
D、如果滤液中含有Ag+,则滤渣中只含有锌和硝酸银反应生成的银,因此滤渣一定为纯净物,该选项说法正确.
故选:C.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.


 习题精选系列答案
习题精选系列答案科目:初中化学 来源:【全国区级联考】广东省深圳市坪山新区2017届九年级下学期第二次调研化学试卷 题型:选择填充题
通过下列化学反应能达到目的是( )
A. 用盐酸除去生石灰中的少量石灰石:CaCO3+2HCl═CaCl2+CO2↑+H2O
B. 用氢氧化铝治疗胃酸过多症:Al(OH)3+HCl=AlCl3+3H2O
C. 在实验室中用碳燃烧制取二氧化碳:C+O2 CO2
CO2
D. 用熟石灰除去NaOH中的Na2CO3:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
查看答案和解析>>
科目:初中化学 来源:2017届山东省日照市莒县九年级下学期第二次学业水平模拟测试化学试卷(解析版) 题型:选择填充题
物质的宏观性质与微观组成(或结构)相互联系是化学特有的思维方式, 下列对物质性质的微观解释不正确的是( )
A. 降温能使水结冰,是因为在较低的温度下水分子静止不动
B. 水和过氧化氢化学性质不同,是因为分子的构成不同
C. 稀有气体的化学性质比较稳定,是因为它们的原子结构都相对稳定
D. 氢氧化钾溶液、石灰水都能使石蕊试液变蓝,是因为它们都含有OH-
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图为电热扇的示意图.
如图为电热扇的示意图.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 ”为铜片).
”为铜片).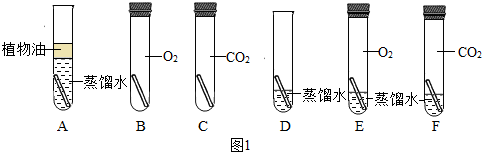
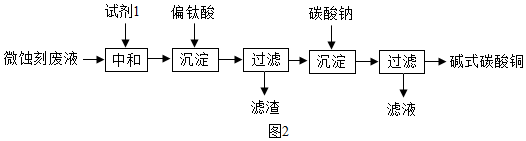
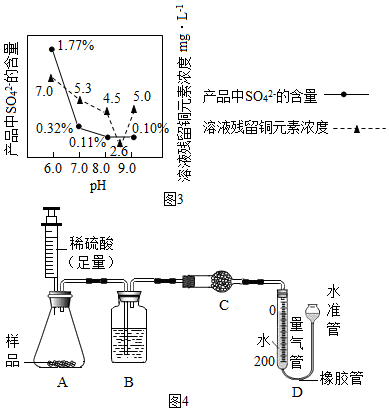
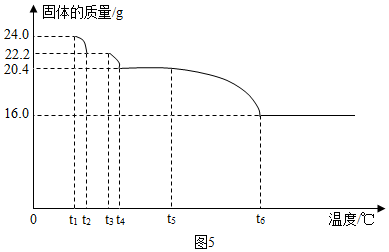
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 河水经过沉淀、过滤、吸附、杀菌消毒等物理净化方法可得到自来水 | |
| B. | 如果将水样蒸干后有固体析出,这种水样中一定含有杂质 | |
| C. | 用直流电电解水,发现负极与正极上得到的气体体积比约为2:1 | |
| D. | 用肥皂水可区分硬水和蒸馏水 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水的电解实验说明水是由氢气和氧气组成的 | |
| B. | 可用肥皂水区分硬水和软水 | |
| C. | 活性炭吸附水中的色素和异味是化学变化 | |
| D. | 用过滤的方法可以使硬水软化 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
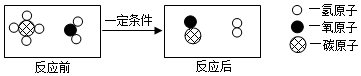
| A. | 该化学反应中有单质生成 | |
| B. | 反应前后各元素的原子个数不变 | |
| C. | 该反应的化学方程式为CH4+H2O$\frac{\underline{\;一定条件\;}}{\;}$CO+H2 | |
| D. | 反应前后分子的数目发生了改变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com