
【题目】某校研究小组对氯酸钾热分解进行以下探究。
[探究一]第一小组通过氧气传感器进行探究,绘制出氧气浓度随温度的变化如图所示。
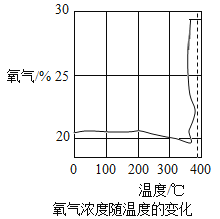
查阅资料:KClO3的熔点约为356°C,MnO2的分解温度约为535°C,用酒精灯给物质加热,受热物质的温度一般约为400°C左右,从图中可知,KClO3分解温度_____(填“>”、“=”或“<”)其熔点。在KCIO3分解前,传感器得到氧气浓度降低的可能原因是____。
[探究二]第二小组发现:氯酸钾与氧化铜混合加热,也能较快产生氧气。于是,按下表进行实验探究,并测定分解温度。
实验编号 | 实验用品 | 分解温度 |
① | 3.0g氯酸钾 | 580 |
② | 3.0g氯酸钾和1.0g二氧化锰 | 350 |
③ | xg氯酸钾和1.0g氧化铜 | 370 |
(1)实验3中x的值应为_____;由对比实验____(填标号),证明氧化铜也会加快氯酸钾的分解,但催化效果更好的物质是_____。
(2)在探究“氧化铜用量与一定质量氯酸钾分解速率关系”时,得出有关实验数据如下:
氧化铜与氯酸钾的质量比 | 1/40 | 1/20 | 1/10 | 1/5 | 1/3 | 1/2 | 2/3 | 1/1 | 2/1 |
生成1L氧气所需的时间(s) | 124 | 79 | 50 | 54 | 75 | 93 | 106 | 153 | 240 |
分析数据:氧化铜与氯酸钾的质量比为____时,反应速率最快。因此,在化学反应中催化剂的用量_____ (填“是”或“不是”)越多越好。
[探究三]第三小组利用氯酸钾和二氧化锰制取氧气时,发现生成的气体略带颜色,并有刺激性气味。
提出问题:生成的气体中除了氧气外还含有什么物质?
查阅资料:①常温下,氯气是黄绿色、二氧化氯是黄色,都有强烈刺激性气味的气体;
②二氧化氯具有强氧化性,可与硫酸锰溶液反应生成不溶于水的二氧化锰,而氯气不能。
提出假设:
假设1:含有氯气;假设2:含有二氧化氯。
设计实验:
实验步骤 | 实验现象 | 实验结论 |
____ | _____ | 假设2正确 |
【答案】> 试管内气压增大,排出一部分空气,而此时氯酸钾还没有分解生成氧气 3.0 ①③ 二氧化锰 1∶10 不是 将生成的气体通人一定量的硫酸锰溶液中 溶液出现黑色浑浊
【解析】
[探究一]
根据图中的数据可知氯酸钾的分解温度大约是380°C,氯酸钾的熔点是356°C,故KClO3分解温度>其熔点;由于加热后实验装置内的空气受热膨胀,会逸出,而此时温度并未达到氯酸钾的分解温度,氯酸钾并未开始产生氧气,导致装置内的氧气浓度降低;
[探究二]
(1)通过实验①氯酸钾的分解温度和实验③氧化铜催化下分解温度的对比可知,氧化铜的存在大大降低了分解温度,加快氯酸钾的分解;要证明不同催化剂对催化效果的影响,就要运用控制变量法进行对比实验的设计,取等量的氯酸钾和等量的不同催化剂,比较氯酸钾的分解温度,故x的数值为3.0,此时二氧化锰催化下氯酸钾的分解温度低于氧化铜催化下分解温度,说明二氧化锰的催化效果更好;
(2)通过表中数据可知,当氧化铜与氯酸钾的质量比为1∶10时,生成1L氧气的时间最短,反应速率最快,再增加氧化铜质量并不会使反应的时间越来越短。因此,在化学反应中催化剂的用量不是越多越好。
[探究三]
根据资料可知,颜色和气味无法鉴别氯气和二氧化氯,因此,寻找两种气体化学性质的不同点,是要将气体通人硫酸锰溶液中,二氧化氯会使二价锰变成四价锰,根据实验现象生成黑色的物质来判定,而氯气不具备这种性质,故将生成的气体通入一定量的硫酸锰溶液中,看到溶液出现黑色浑浊,就能证明假设2正确。


科目:初中化学 来源: 题型:
【题目】氢氧化钠与稀盐酸反应观察不到明显现象,为了确定反应是否发生,丽丽小组同学设计了如下图所示的实验探究方案。
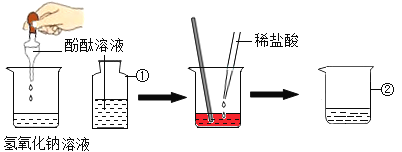
请回答下列问题:
(1)标号仪器的名称:①_____,②_____。
(2)玻璃棒在实验中的作用及目的_____。
(3)当观察到烧杯中溶液颜色_____时,说明酸碱恰好中和反应。
(4)该实验过程中发生反应的化学力程式_____。
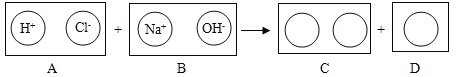
(5)仿照填写下用圆圈内的空白,其反应的实质是_____。
(6)若将50g质量分数7.3%的稀盐酸与50g质量分数8%的氢氧化钠溶液充分后,反应所得溶液的溶质质量分数是_____。
(7)酸、碱,盐水溶液导电是因为它们在水中溶解时能产成自由移动的离子,这个过程叫做电离。试着写出氢氧化钠的电离方程式_____。
(8)下列关于该实验方案中,能证明氢氧化钠与盐酸发生反应的序号是_____。
A 用pH试纸测定氢氧化钠溶液的pH,然后向其中滴加稀盐酸,测得溶液的pH逐渐减小,最终小于7
B 用温度计测量氢氧化钠溶液在滴加稀盐酸前与后的温度,发现其明显上升
C 蒸发反应后所得的无色溶液得到白色的固体
D 向一定量NaOH溶液被中滴加稀盐酸、再滴加硫酸铜溶液,有蓝色沉淀生成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】按要求填空:
(1)空气中含量最多的气体___________(填化学式),标出氯酸钾中氯元素的化合价____________。
(2)下表列出的是某品种西瓜每100g食用部分的主要营养成分数据。
营养成分 | 水分 | 蛋白质 | 脂肪 | 糖类 | X | 钙铁锌 |
质量 | 92.5g | 0.7g | 0.2g | 6.1g | 6.8mg | 17.1mg |
表中“X”是指人体所需六大基本营养素中的_________,西瓜中含有的__________元素可预防贫血。
(3)图中表示氧化汞分子受热分解发生反应的示意图:

根据上图你能获得的信息有:_______________(填符合题意的2条即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2018年5月9日,我国“高分五号”卫星发射成功。
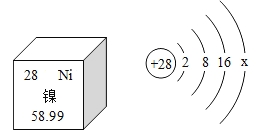
(1)高氯酸钾(KClO4)可用作火箭燃料,其中氯元素的化合价为______。
(2)钛镍形状记忆合金可制作卫星天线。如图是镍元素在元素周期表中的信息以及原子结构示意图。镍元素的相对原子质量为_____,X的数值是_____,在化学反应中容易_____(填“失去”或“得到”)电子。
(3)“高分五号”是我国首颗对大气中二氧化硫、二氧化氮、二氧化碳、甲烷等多个环境要素进行监测的卫星。
①上述四种气体可以造成酸雨的是_____(写一种)。
②催化还原法是消除大气中氮氧化物污染的新工艺,反应微观示意图如图,写出反应的化学方程式:____。
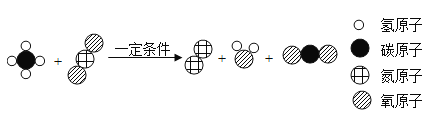
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如今,走向“地铁、高铁时代”的中国,正大力发展电气化铁路。高铁的运行为我们的出行提供了方便。中国的高铁技术不仅服务于中国,也终将造福于全人类。请试着回答下列问题:

(1)地铁、高铁的车身具有密度小,抗腐蚀性好的性质,应选择的合金_____;(在A、B、C中选填)
A 锰钢 B 铝合金 C 不锈钢
(2)高铁在工作过程中的能量转化为_____;
(3)高铁运行时的接触材料用铜及铜合金线,而火法炼铜是当今生产铜的主要方法。其中重要的一步是用氧化亚铜(Cu2O)和硫化亚铜(Cu2S)高温反应生成高纯度的铜和一种气态空气污染物,则发生反应的化学方程式是_____,该反应前后铜元素的化合价变化为_____。
(4)地铁的建成将大大缓解城市的交通压力并保护环境,将减少汽车污染物的排放,如一氧化碳、未燃烧的碳氢化合物、_____、含铅化合物、_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钾和硝酸钾晶体在不同温度时的溶解度如表所示:
温度/℃ 溶解度/g 物质 | 0 | 10 | 20 | 30 | 40 |
KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 |
KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 |
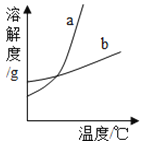
(1)30℃时,硝酸钾的溶解度为_____;
(2)等质量这两种物质的饱和溶液从40℃降温到10℃时析出晶体更多的是_____;
(3)若两种物质的溶解度相等,此时所对应的温度范围在_____之间;
(4)如图中能表示KCl溶解度曲线的是(填“a”或“b”)_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生铁是铁和碳的合金.为测定某炼铁厂生产的生铁样品中铁的质量分数,化学兴趣小组的同学称得该生铁样品6.0g,放入烧杯中,向其中加入65.0g稀硫酸,恰好完全反应(假设杂质不参与反应).测得的实验数据如下:
反应前 | 反应后 | |
烧杯及其中物质的质量 | 97.0g | 96.8g |
请你完成有关计算(结果保留一位小数):
(1)反应放出的氢气是多少?
(2)生铁样品中铁的质量分数是多少?
(3)反应后所得溶液的质量是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是一组用于研究可燃物燃烧条件的对比实验,对有关实验现象和结论的判断错误的是( )
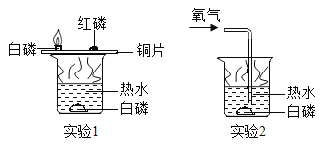
A.实验1中红磷未燃烧,说明红磷的着火点高于白磷
B.实验2中白磷燃烧,说明实验2中的热水温度高于实验1
C.实验2中如果停止通入氧气,燃着的白磷会熄灭
D.可燃物燃烧需要氧气(或空气),并且周围温度达到着火点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com