
| 次数 | 第1次 | 第2次 | 第3次 | 第4次 |
| 滴加盐酸的质量(g) | 25 | 25 | 25 | 25 |
| 产生气体的质量(g) | 2.2 | 4.4 | 4.4 | 4.4 |
分析 (1)根据表中的数据分析氢氧化钠、碳酸钠与盐酸的反应;
(2)根据二氧化碳的质量求出碳酸钠的质量、生成氯化钠的质量,根据碳酸钠的质量求出氢氧化钠的质量,即可求出样品中氢氧化钠的质量分数;
(3)根据氢氧化钠的质量求出生成的氯化钠的质量,再根据溶质的质量分数计算恰好完全反应后溶液的溶质的质量分数.
解答 解:(1)由表中的数据可知,每25g的盐酸与碳酸钠反应生成了2.2g 的气体,第二次加入25g 的盐酸时恰好完全反应.
(2)设碳酸钠的质量为x,生成的氯化钠的质量为y.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 4.4g
$\frac{106}{x}=\frac{117}{y}=\frac{44}{4.4g}$ 解得:x=10.6gy=11.7g
样品中氢氧化钠的质量分数是:$\frac{20g-10.6g}{20g}×100%$=47%
(3)设氢氧化钠与盐酸反应生成氯化钠的质量为z.
HCl+NaOH=NaCl+H2O
40 58.5
9.4g z
$\frac{40}{58.5}=\frac{9.4g}{z}$ 解得:z≈13.7g
恰好完全反应后溶液的溶质的质量分数是:$\frac{11.7g+13.7g}{20g+100g+50g-4.4g}×100%$≈15.3%
答:(1)2;(2)样品中氢氧化钠的质量分数为47%;(3)恰好完全反应后溶液的溶质质量分数为15.3%.
点评 本题属于根据化学方程式和溶质质量分数的综合计算题,根据表中的数据对比分析出生成的二氧化碳的质量是解答本题的关键.


科目:初中化学 来源: 题型:解答题
| 生活用品 | 洗发液 | “84”消毒液 | 洁厕灵 | 炉灶清洁剂 |
| 有效成分 | 表面活性剂 | 次氯酸钠 | 盐酸 | 氢氧化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 冶炼方法 | 主要原理 | 代表金属 |
| 电解法 | 熔融的金属化合物在通电的条件下分解 | 钠、铝 |
| 热还原法 | 金属氧化物与一氧化碳(或碳等)在高温的条件下反应 | 铁、铜 |
| 热分解法 | 金属氧化物在加热的条件下分解 | 汞、银 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
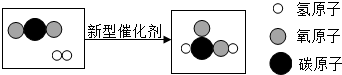
| A. | 反应前后原子总数减少 | B. | 反应物和生成物中共有两种氧化物 | ||
| C. | 可用于减少温室气体的排放 | D. | 得到的液体燃料化学式是H2C2O |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如图为某反应的微观示意图,该反应中化合价发生改变的元素是氯元素,将反应后的溶液稀释,溶液的pH会变大(选填“变大”“变小”或“不变”),若将反应后溶液与NaOH恰好完全反应,所得溶液中溶质为NaCl和NaClO.
如图为某反应的微观示意图,该反应中化合价发生改变的元素是氯元素,将反应后的溶液稀释,溶液的pH会变大(选填“变大”“变小”或“不变”),若将反应后溶液与NaOH恰好完全反应,所得溶液中溶质为NaCl和NaClO.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图表示某些物质间转化关系(反应条件和部分产物已省略),其中A、E为固体氧化物,且A为黑色粉末;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;C、Y、Z为无色气体,其中Y有毒;X是最常见的金属.
如图表示某些物质间转化关系(反应条件和部分产物已省略),其中A、E为固体氧化物,且A为黑色粉末;B、D是由相同元素组成的无色液体,且B具有消毒杀菌作用;C、Y、Z为无色气体,其中Y有毒;X是最常见的金属.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com