
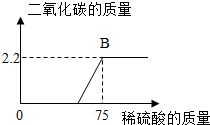
 某化工厂排放的废水中含有碳酸钾和氢氧化钾,化学兴趣小组为探究废水中碳酸钾的含量,提取50g废水样品于集气瓶中,逐滴加入9.8%的稀硫酸,反应过程中产生二氧化碳的质量与加入稀硫酸的质量如下图,请计算:
某化工厂排放的废水中含有碳酸钾和氢氧化钾,化学兴趣小组为探究废水中碳酸钾的含量,提取50g废水样品于集气瓶中,逐滴加入9.8%的稀硫酸,反应过程中产生二氧化碳的质量与加入稀硫酸的质量如下图,请计算:分析 (1)根据图象分析判断;
(2)先根据二氧化碳的质量结合化学方程式计算出废水中碳酸钾的质量和与碳酸钾反应的硫酸的质量,利用质量差即可计算出氢氧化钾消耗的硫酸质量,根据硫酸与氢氧化钾反应的化学方程式即可解答
解答 解:(1)根据图象分析判断,生成二氧化碳的质量为:2.2g;
(2)设废水中碳酸钾的质量为x,
K2CO3+H2SO4=K2SO4+H2O+CO2↑;
138 44
x 2.2g
$\frac{138}{x}$=$\frac{44}{2.2g}$
x=6.9g
该废水中碳酸钾的质量分数是:$\frac{6.9g}{50g}$×100%=13.8%,
答:该废水中碳酸钾的质量分数是13.8%.
点评 解答本题的关键是利用质量守恒定律和利用化学方程式计算.


科目:初中化学 来源: 题型:填空题
| 实验方案 | ①测溶液pH | ②滴加Na2CO3溶液 | ③滴加BaCl2溶液 |
| 实验现象 | 试纸变色,与标准比色卡比照,得pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 紫色石蕊试液 | B. | 无色酚酞试液 | C. | pH试纸 | D. | 闻气味 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com