
【题目】根据要求回答问题。
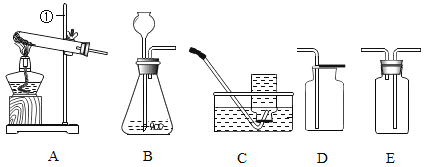
(1)写出仪器①的名称___________________。
(2)用氯酸钾和二氧化锰制取氧气的化学方程式为___________,该反应属于_____________(填基本反应类型),二氧化锰的作用是___________。 用装置C收得的氧气不纯,可能的原因是___________。
(3)实验室用稀盐酸和石灰石制取CO2,选用的发生装置是___________, 反应的化学方程式为___________。将气体通过盛有___________的E装置,可得到干燥的CO2。
(4)为验证可燃物燃烧需要氧气,某同学利用中间凹陷的软质塑料瓶设计如下实验。
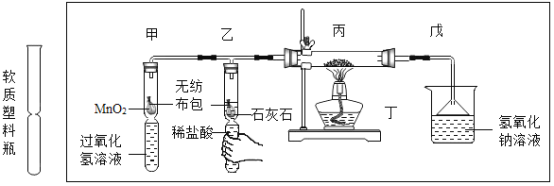
①通过捏放软塑料瓶下端可控制_______________。
②实验步骤:先捏住乙处瓶身一段时间(如图所示),后点燃丁处酒精灯,观察到丙处无明显变化;放开乙处瓶身,____________(填具体操作),丙中红磷燃烧,产生白烟。结论:燃烧需要氧气。实验中,先捏住乙处瓶身一段时间的目的是_____________。
③戊中氢氧化钠溶液可吸收有毒的五氧化二磷,生成磷酸钠(Na3PO4)和水,反应的化学方程式为_____________。
【答案】铁架台 2KClO3![]() 2KCl+3O2↑ 分解反应 催化作用 导管口一有气泡冒出就开始收集或集气瓶内留有气泡等 B CaCO3+2HCl=CaCl2+H2O+CO2↑ 浓硫酸 反应的发生与停止 捏住甲处瓶身下半部分一段时间 排除装置的空气与后面要做的实验形成对比 6NaOH+P2O5=2Na3PO4+3H2O
2KCl+3O2↑ 分解反应 催化作用 导管口一有气泡冒出就开始收集或集气瓶内留有气泡等 B CaCO3+2HCl=CaCl2+H2O+CO2↑ 浓硫酸 反应的发生与停止 捏住甲处瓶身下半部分一段时间 排除装置的空气与后面要做的实验形成对比 6NaOH+P2O5=2Na3PO4+3H2O
【解析】
(1)仪器①的名称:铁架台;
(2)氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,化学方程式为:2KClO3![]() 2KCl+3O2↑;符合“一变多”的特点,是分解反应;在这个反应中二氧化锰起催化作用;用装置C收得的氧气不纯,可能的原因是:导管口一有气泡冒出就开始收集或集气瓶内留有气泡等;
2KCl+3O2↑;符合“一变多”的特点,是分解反应;在这个反应中二氧化锰起催化作用;用装置C收得的氧气不纯,可能的原因是:导管口一有气泡冒出就开始收集或集气瓶内留有气泡等;
(3)实验室用稀盐酸和石灰石制取CO2,不需要加热,可选用B装置作发生装置;化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳不和浓硫酸反应,可以用浓硫酸干燥二氧化碳;所以将气体通过盛有的浓硫酸E装置,可得到干燥的CO2;
(4)①根据装置的特点可知,通过捏放软塑料瓶下端可控制反应的发生与停止;
②根据控制变量实验法的方法可知,先捏住乙处瓶身一段时间(如图所示),后点燃丁处酒精灯,观察到丙处无明显变化;放开乙处瓶身,捏住甲处瓶身下半部分一段时间,丙中红磷燃烧,产生白烟;实验中,捏住乙处瓶身一段时间的目的是排除装置的空气与后面要做的实验形成对比;
③五氧化二磷和氢氧化钠反应生成磷酸钠和水,化学方程式为:6NaOH+P2O5=2Na3PO4+3H2O。
故答案为:
(1)铁架台;
(2)2KClO3![]() 2KCl+3O2↑;分解反应;催化作用;导管口一有气泡冒出就开始收集或集气瓶内留有气泡等;
2KCl+3O2↑;分解反应;催化作用;导管口一有气泡冒出就开始收集或集气瓶内留有气泡等;
(3)B;CaCO3+2HCl=CaCl2+H2O+CO2↑;浓硫酸;
(4)①反应的发生与停止;
②先捏住甲处瓶身下半部分一段时间;排除装置的空气与后面要做的实验形成对比;
③6NaOH+P2O5=2Na3PO4+3H2O。


科目:初中化学 来源: 题型:
【题目】同学们对“影响金属与盐酸反应剧烈程度的因素”进行了探究。
[提出问题]金属与盐酸反应剧烈程度受哪些因素影响?
[做出猜想] Ⅰ.与盐酸的浓度有关Ⅱ .与____________有关Ⅲ.与金属的种类有关
[进行实验]
实验编号 | 金属 | 盐酸的质量分数% | 温度℃ | 金属丝消失的时间s |
① | 铝丝 | 5 | 20 | 450 |
② | 铝丝 | 8 | 20 | t |
③ | 铝丝 | 10 | 20 | 240 |
④ | 铝丝 | 10 | 30 | 65 |
⑤ | 铁片 | 10 | 30 | 125 |
[解释与结论]
(1)补充猜想:金属与盐酸反应剧烈程度,与____________有关。
(2)铝与盐酸反应的方程式为_________________。
(3)由实验①③可知,猜想1___________。(填“成立”或“不成立”)。在实验②中,铝丝消失的时间(用t表示)的取值范围是_________________。
(4)有同学认为通过实验④⑤并不能证明“猜想与假设Ⅲ”成立,理由是_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一种新型火箭推进剂在火箭发射过程中,发生反应的微观过程如图所示,下列有关说法不正确的是( )

A.反应前后原子种类不变,分子种类发生了改变
B.该反应前后一定有元素的化合价发生改变
C.参加反应的甲、乙与生成的丙、丁的分子个数比为1:2:3:4
D.上述四种物质中属于氧化物的有三种
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】锶元素的相关信息如图所示,下列说法正确的是
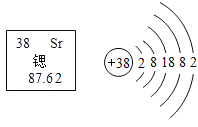
A.锶原子核外电子数是2
B.锶元素属于金属元素
C.锶的相对原子质量是87.62g
D.锶的化学性质较稳定
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】牙膏是一种日用必需品。某兴趣小组对某一品牌牙膏中所含摩擦剂的成分进行了如下探究。
[查阅资料]
(1)常用的牙膏摩擦剂的主要成分有CaCO3、Al(OH)3、SiO2。
(2)牙膏中除了碳酸钙以外,其他物质均不与稀盐酸反应产生气体。
(3)SiO2不溶于水,也不与盐酸反应。氢氧化铝和稀盐酸可以发生中和反应。
(4)AI(OH)3能和氢氧化钠溶液发生反应,该反应的化学方程式为:Al(OH)3+NaOH=NaAlO2+2_____(填化学式)
[提出问题]:该品牌牙膏的酸碱性如何?其中含有什么摩擦剂?
[实验与猜想]
(1)取少量牙膏膏体于小烧杯中,加入10毫升蒸馏水,充分搅拌,静置一段时间,分离上层清液和沉淀;
(2)用____(填字母)测定所得溶液的pH值大于7。
A pH试纸
B 紫色石蕊试液
C 酚酞试液
(3)取少量沉淀物加入过量的稀盐酸,沉淀物全部溶解并有大量气泡产生,同时得到澄清溶液,如图所示,则该品牌牙膏中一定含有碳酸钙,一定不含有_____。
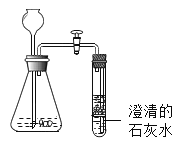
(4)进行猜想:摩擦剂成分可能是a.只含碳酸钙b._____。
[设计实验]同学们为进一步 确认摩擦剂中含有氢氧化铝,进行了如下实验:
实验步骤 | 实验现象 | 解释与结论 |
取实验(3)中锥形瓶内反应后的澄清溶液,逐滴滴入定量氢氧化钠溶液 | 开始无明显现象,后产生大量白色沉淀 | 开始无明显现象,是因为开始时加入的氢氧化钠溶液和过量的____反应。继续滴入氢氧化钠化钠溶液后产生白色沉淀原因是_____(用化学方程式表示) |
继续滴入氢氧化钠溶液至过量 | 白色沉淀溶解 | 摩擦剂中还含有氢氧化铝 |
[实验结论]该牙膏摩擦剂成分可以确定。
[总结与提升]判断混合物中物质成分时,除了要考虑生成物,还要考虑_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某班学生分三组分别做了二氧化碳制取和性质验证实验,如下图所示。

甲 乙 丙
实验结束后,老师取两份等质量的丙废液,分别与甲、乙废液混合。将甲废液与丙废液倒入烧杯A中,有白色沉淀生成;将乙废液与丙废液倒入烧杯B中,有气泡产生。
请填空:
(1)甲废液与乙废液所含溶质的成分可能不同的是 (用化学式填空,下同)。
(2)烧杯A中沉淀的成分一定有 。
(3)另取少量丙废液样品,加入足量的氯化钡溶液,有白色沉淀生成。过滤,向滤液中滴加氯化铁溶液,观察到有红褐色沉淀生成,未发现其他明显现象。
由此推测出,丙废液溶质的成分是 ,丙废液与氯化钡溶液反应的化学方程式为 ,烧杯A的上层清液中溶质的成分一定有 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】青岛是美丽的沿海城市,海水资源丰富,海水晒盐可以得到粗盐,粗盐中含有泥沙等不溶性杂质,可能含MgCl2、CaCl2 和Na2SO4等可溶性杂质,某同学设计如下实验方案提纯粗盐,同时验证可溶性杂质是否存在。
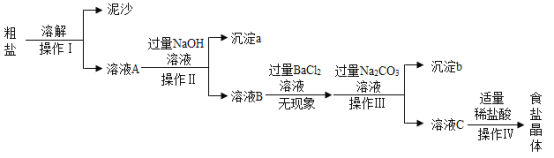
对该过程的认识中,正确的是( )
A.Ⅰ操作中需要进行搅拌,目的是提高氯化钠的溶解度
B.Ⅱ、Ⅲ两步操作顺序可以颠倒
C.沉淀b中共有三种物质
D.最后还要加入适量盐酸,加入盐酸的目的是除去过量的氢氧化钠和碳酸钠,将滤液的pH调为7
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2019年是国际元素周期表年。俄国化学家门捷列夫在公布元素周期表时,就预言了当时还未发现的相对原子质量约为68的元素的存在,且性质与铝相似,称为“类铝”。如图是元素周期表中“类铝”元素镓的相关信息,回答下列问题:
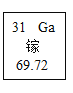
(1)镓原子核外电子数为_____。
(2)金属镓与稀硫酸反应,产物中Ga的化合价为+3,反应的化学方程式为_____。可推测镓在金属活动性顺序里位于_____ (填“氢前”“氢后”)。
(3)高纯氧化镓广泛用于生产半导体材料,制高纯氧化镓的第一步是向含有硫酸的硫酸镓溶液中通入氨气(NH3),冷却,生成Ga (NH4) (SO4)2固体。Ga (NH4)(SO4)2中含有的带正电荷的原子团(根)是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为A、B、C三种物质的溶解度曲线,回答下列问题。
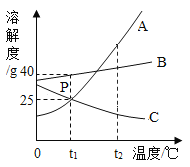
(1)当温度在t1℃<t<t2℃之间时,A物质与B物质_____ (填“能”或“不能”)配制溶质质量分数相同的饱和溶液。
(2) t1℃时,若要将210克B物质的饱和溶液稀释成溶质质量分数为10%的溶液,需要加水的质量为_____。
(3)分别将A、B、C的饱和溶液从t2℃降温至t1℃,所得溶液中溶质质量分数的大小关系是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com