
| A、这个反应属于复分解反应 | B、NaHCO3一定是难溶于水的物质 | C、反应后的溶液中存在NH4+ | D、结晶出NaHCO3后的溶液中没有Na+ |
科目:初中化学 来源: 题型:
| A、图书馆图书着火时,立刻用液态二氧化碳灭火器来灭火 | B、厨房液化气泄漏 引起火灾时,就开窗通风换气 | C、油井着火时,就设法降低油的着火点 | D、电器设备失火时,应用水灭火 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、海洋是个巨大的资源库,人们可以无节制的向她索取各种资源 | B、海水“晒盐”是利用蒸发结晶的方法从海水中得到食盐 | C、海洋本身就是个巨大的水资源库,如何获取廉价的淡水对缓解淡水危机意义重大 | D、海水“制碱”是利用向饱和氨盐水中通入二氧化碳过滤,加热过滤后固体得到纯碱 |
查看答案和解析>>
科目:初中化学 来源: 题型:
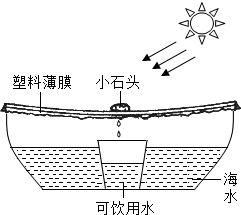 海水是种宝贵资源.
海水是种宝贵资源.| 温度(℃) | 0 | 20 | 40 | 60 | 80 |
| 溶解度(g/100g水) | 3 | 5 | 9 | 15 | 23 |
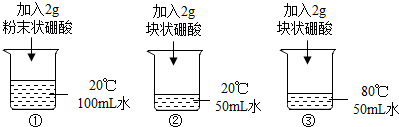
查看答案和解析>>
科目:初中化学 来源: 题型:
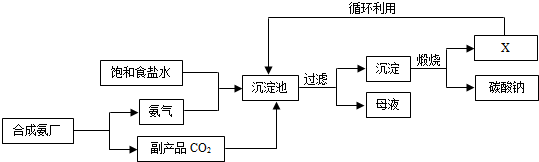
| A、沉淀池中得到的沉淀是NaHCO3,因为该条件下NaHCO3的溶解度比NH4Cl小 | B、过滤得到的“母液”中一定只含有两种溶质 | C、图中X可能是氨气 | D、通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com