
”¾ĢāÄæ”æČēĶ¼ĪŖ”°XX”±øĘʬÉĢĘ·±źĒ©Ķ¼£¬Ēėøł¾Ż±źĒ©µÄÓŠ¹ŲŠÅĻ¢Ķź³ÉĻĀĮŠø÷Ģā”£

(1)ĆæʬøĘʬ֊ŗ¬øĘŌŖĖŲµÄÖŹĮæÖĮÉŁĪŖ___æĖ
(2)Š”ŗģĶ¬Ń§ĪŖ²ā¶ØĘäÖŠĢ¼ĖįøʵÄŗ¬Įæ±ź×¢ŹĒ·ńŹōŹµ£¬ĖżČ”³ö10ʬøĘʬ£¬ŃŠĖéŗó·ÅČėŠ”ÉÕ±ÖŠ£¬ŌŁ¼ÓČė50gĻ”ŃĪĖį£¬ŌŚT0ÖĮT3Ź±¼ä¶Ī£¬²āµĆ·“Ó¦Ź£ÓąĪļµÄÖŹĮæ±ä»ÆČēĻĀ£ŗ
Ź±¼ä | T0 | T1 | T2 | T3 |
·“Ó¦Ź£ÓąĪļÖŹĮæ(g) | 70 | 65 | 63.4 | 63.4 |
¢ŁÉś³ÉµÄ¶žŃõ»ÆĢ¼µÄÖŹĮæŹĒ___æĖ£»
¢ŚĶعż¼ĘĖćÅŠ¶ĻøĆøĘʬ֊Ģ¼ĖįøʵÄŗ¬Įæ±ź×¢ŹĒ·ńŹōŹµ___”£(Š“³ö¼ĘĖć¹ż³Ģ)
”¾“š°ø”æ0.6 6.6 øĆøĘʬ֊Ģ¼ĖįøʵÄŗ¬Įæ±ź×¢ŹōŹµ
”¾½āĪö”æ
(1) ĆæʬøĘʬ֊ŗ¬Ģ¼ĖįøĘ![]() 1.5g£¬øĘŌŖĖŲµÄÖŹĮæ=Ģ¼ĖįøʵÄÖŹĮæ
1.5g£¬øĘŌŖĖŲµÄÖŹĮæ=Ģ¼ĖįøʵÄÖŹĮæ![]() øĘŌŖĖŲµÄÖŹĮæ·ÖŹż£»
øĘŌŖĖŲµÄÖŹĮæ·ÖŹż£»
(2) ¢ŁT2”¢T3·“Ó¦Ź£ÓąĪļÖŹĮæ(g)ĻąµČ£¬ĖµĆ÷Ģ¼ĖįøĘŅŃ¾ĶźČ«·Ö½ā£¬ŌŁøł¾ŻÖŹĮæŹŲŗć¶ØĀÉ£¬ĒóµĆ¶žŃõ»ÆĢ¼µÄÖŹĮ棻
¢Śøł¾Ż»Æѧ·½³ĢŹ½CaCO3+2HClØTCaCl2+H2O+CO2”üæÉĒóµĆĢ¼ĖįøʵÄÖŹĮ棬ŌŁ±Č½Ļæ“ŹĒ·ńĆæʬøĘʬ֊ŗ¬Ģ¼ĖįøĘ![]() 1.5g”£
1.5gӣ
(1)ĆæʬøĘʬ֊ŗ¬Ģ¼ĖįøʵÄÖŹĮæÖĮÉŁ1.5g£¬ĖłŅŌøĘŌŖĖŲµÄÖŹĮæÖĮÉŁĪŖ![]() £»
£»
(2)øł¾ŻÖŹĮæŹŲŗć¶ØĀÉ£¬¶žŃõ»ÆĢ¼µÄÖŹĮæĪŖ£ŗ2g”Į10+50g©36.4g£½6.6g
ÉčĆæʬøĘʬŗ¬ÓŠµÄĢ¼ĖįøʵÄÖŹĮæĪŖx”£
CaCO3+2HClØTCaCl2+H2O+CO2”ü
100 44
10x 6.6g
![]()
x£½1.5g
Óė±źĒ©±£³ÖŅ»ÖĀ”£
“š£ŗ(1)ĆæʬøĘʬ֊ŗ¬øĘŌŖĖŲµÄÖŹĮæÖĮÉŁĪŖ0.6æĖ
(2)¢Ł¶žŃõ»ÆĢ¼µÄÖŹĮæŹĒ6.6æĖ£»
¢ŚøĆøĘʬ֊Ģ¼ĖįøʵÄŗ¬Įæ±ź×¢ŹōŹµ”£


 ĘŚÄ©ŗĆ³É¼ØĻµĮŠ“š°ø
ĘŚÄ©ŗĆ³É¼ØĻµĮŠ“š°ø 99¼Ó1ĮģĻČĘŚÄ©ĢŲѵ¾ķĻµĮŠ“š°ø
99¼Ó1ĮģĻČĘŚÄ©ĢŲѵ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĪŅ¹ś»Æѧ¼ŅŗīµĀ°ń·¢Ć÷ĮĖĮŖŗĻÖĘ¼ī·Ø£¬ĘäÉś²ś“æ¼īŗĶø±²śĘ·ĀČ»Æļ§µÄ¹¤ŅÕĮ÷³ĢČēĶ¼1ĖłŹ¾£ŗ
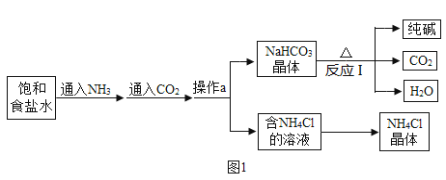
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³ö·“Ó¦IµÄ»Æѧ·½³ĢŹ½£ŗ_____£¬ŗ¬NH4ClµÄČÜŅŗµĆµ½NH4Cl¾§ĢåµÄ¹ż³ĢŹĒ¼ÓČČÅØĖõ”¢_____”¢¹żĀĖ”£
£Ø2£©ÉĻŹö¹¤ŅÕĮ÷³ĢÖŠæÉŃ»·ĄūÓƵÄĪļÖŹŹĒ_____”£
£Ø3£©ļ§ŃĪĖ®ĪüŹÕ¶žŃõ»ÆĢ¼ŗóÉś³ÉĢ¼ĖįĒāÄĘŗĶĀČ»Æļ§£¬Ģ¼ĖįĒāÄĘŹ×ĻČ½į¾§Īö³ö£¬ŌŅņŹĒ_____”£
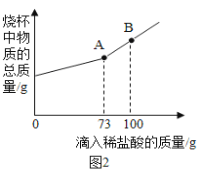
£Ø4£©Ä³ÖĘ¼ī³§ÖĘ³öµÄNa2CO3ŗ¬ÓŠNaCl£¬Č”12gøĆѳʷ·ÅČėÉÕ±ÖŠ£¬Öš½„µĪ¼ÓČÜÖŹÖŹĮæ·ÖŹżĪŖ10%µÄĻ”ŃĪĖį£¬ÉÕ±ÖŠĪļÖŹµÄ×ÜÖŹĮæÓėĖłµĪČėĻ”ŃĪĖįµÄÖŹĮæ¹ŲĻµĒśĻßČēĶ¼2ĖłŹ¾£¬Ēė¼ĘĖćѳʷ֊Na2CO3µÄÖŹĮæ·ÖŹż£Ø½į¹ū±£Įō1Ī»Š”Źż£©_____”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¼×”¢ŅŅ”¢±ūČżÖÖĪļÖŹŌŚĖ®ÖŠŠĪ³ÉµÄ±„ŗĶČÜŅŗČÜÖŹÖŹĮæ·ÖŹżĖęĪĀ¶Č±ä»ÆČēĻĀĶ¼ĖłŹ¾£¬Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
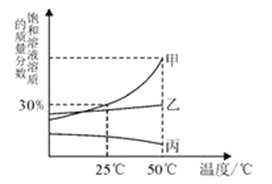
£Ø1£©25”ꏱ£¬¼×ĪļÖŹÖŠµÄČܽā¶ČĪŖ______g£Ø“š°ø±£ĮōŅ»Ī»Š”Źż£©£»
£Ø2£©“ÓŅŅČÜŅŗÖŠ»ńµĆŅŅ¾§ĢåµÄ·½·ØŹĒ_____________£ØĢī”°Õō·¢½į¾§”±»ņ”°½µĪĀ½į¾§”±£©”£
£Ø3£©½«50”ę¼×µÄ±„ŗĶČÜŅŗ½µĪĀÖĮ25”ę£¬ČÜŅŗĪŖ________£ØĢī”°±„ŗĶČÜŅŗ”±»ņ”°²»±„ŗĶČÜŅŗ”±£©”£
£Ø4£©ĘųĢåµÄČܽā¶ČĖęĪĀ¶ČµÄ±ä»Æ¹ęĀÉÓė_________£ØĢī”°¼×”±”¢”°ŅŅ”±»ņ”°±ū”±£©ĻąĖĘ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»ÆѧŹĒŅ»ĆÅŅŌŹµŃéĪŖ»ł“”µÄæĘѧ£¬Ēėøł¾ŻŅŖĒó»Ų“šĪŹĢā”£
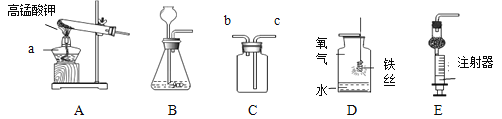
£Ø1£©ŅĒĘ÷aµÄĆū³ĘŹĒ______”£
£Ø2£© ŹµŃéŹŅÓĆ×°ÖĆAÖĘČ”O2Ź±Ó¦×öµÄøĽųĪŖ______”£×°ÖĆDÖŠĖ®µÄ×÷ÓĆŹĒ______”£
£Ø3£©ŹµŃéŹŅÖĘČ”O2”¢H2¾łæÉŃ”Ōń______£ØĢī×°ÖĆŠņŗÅ£©×÷ĪŖĘųĢåµÄ·¢Éś×°ÖĆ”£ŹµŃéŹŅÖĘČ”CO2µÄ»Æѧ·½³ĢŹ½ĪŖ______£¬ČōÓĆ×°ÖĆCŹÕ¼ÆCO2£¬ŃéĀśµÄ·½·ØŹĒ______”£ÓĆ×°ÖĆEÖĘČ”CO2Ź±£¬Ź¹·“Ó¦Ķ£Ö¹µÄ²Ł×÷ŹĒ______”£
£Ø4£©N2ŌŚ¼ÓČČŗĶ“߻ƼĮĢõ¼žĻĀÄÜÓė H2»ÆŗĻÉś³ÉNH3£¬ČēĶ¼ĪŖÖĘȔɣĮæNH3µÄ×°ÖĆ”£
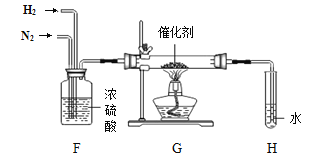
¢Ł¼ģŃéÓŠNH3Éś³ÉµÄ²Ł×÷ŹĒ______”£
¢ŚN2ŗĶH2·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ______”£
¢ŪŅŃÖŖ£ŗĶ¬ĪĀĶ¬Ń¹ĻĀ£¬ĘųĢåµÄĢå»ż±ČµČÓŚ·Ö×ÓŹżÖ®±Č”£Ķ¼ÖŠF×°ÖƵÄ×÷ÓĆÓŠČżµć£ŗŅ»ŹĒøÉŌļN2ŗĶH2£»¶žŹĒŹ¹N2ŗĶH2³ä·Ö»ģŗĻ£»ČżŹĒ______£¬“Ó¶ųĢįøßN2ŗĶH2µÄĄūÓĆĀŹ”£
¢ÜŹµŃé¹²ĻūŗÄ0.4g H2£¬ČōH2ÓÉŠæŗĶČÜÖŹÖŹĮæ·ÖŹżĪŖ20%µÄĻ”ĮņĖį·“Ó¦²śÉś£¬ĒóĻūŗĵÄĻ”ĮņĖįµÄÖŹĮæ______”££ØŠ“³ö½āĢā¹ż³Ģ£©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŖŹ¹ČēĶ¼×°ÖĆÖŠµÄŠ”ĘųĒņ¹ÄĘšĄ“£¬ŌņŹ¹ÓĆµÄ¹ĢĢåŗĶŅŗĢåæÉŅŌŹĒ( )
¢ŁŠæŗĶĻ”ĮņĖį£»¢ŚŹÆ»ŅŹÆŗĶŃĪĖį£»¢ŪĻõĖįļ§ŗĶĖ®£»¢Ü¹ĢĢåĒāŃõ»ÆÄĘŗĶĖ®
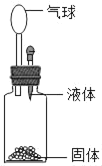
A. ¢Ł¢ŚB. ¢Ł¢Ś¢ÜC. ¢Ł¢ÜD. ¢Ł¢Ū¢Ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĒå»Ŗ“óѧъ¾æČĖŌ±³É¹¦ŃŠÖĘ³öŅ»ÖÖÄÉĆ×ĻĖĪ¬“߻ƼĮ£¬æÉŅŌ½«¶žŃõ»ÆĢ¼×Ŗ»Æ³ÉŅŗĢåČ¼ĮĻ¼×“¼£¬ĘäĪ¢¹ŪŹ¾ŅāĶ¼ČēĶ¼£ØĶ¼ÖŠµÄĪ¢Į£Ē”ŗĆĶźČ«·“Ó¦£©”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A. ¶”µÄ»ÆѧŹ½ĪŖH2O2
B. ²Ī¼Ó·“Ó¦µÄ¼×”¢ŅŅĮ½ĪļÖŹµÄÖŹĮæ±ČĪŖ2£ŗ44
C. øĆ·“Ó¦ŹōÓŚÖĆ»»·“Ó¦
D. “Ė·“Ó¦Éę¼°µÄĖÄÖÖĪļÖŹ¾łÓÉ·Ö×Ó¹¹³É
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潚ŹōŹĒÉś²śÉś»īÖŠÖŲŅŖµÄ²ÄĮĻ”£

£Ø1£©ČēĶ¼1ŹĒĀĮŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄŠÅĻ¢£¬ĘäĻą¶ŌŌ×ÓÖŹĮæŹĒ_____£»ĀĮŌŖĖŲŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĶ¼2£¬ÄĒĆ“aŌŖĖŲŹĒ_____£ØŠ“ŌŖĖŲĆū³Ę£©”£
£Ø2£©×öĢśĖæČ¼ÉÕµÄŹµŃ鏱£¬×öĮĖČēĶ¼3ĖłŹ¾µÄŹµŃ飬·¢ĻÖAÖŠĢśĖæČ¼ÉÕ£¬BÖŠĢśĖæ²»Č¼ÉÕ£¬ĘäŌŅņŹĒ_____”£A¼ÆĘųĘæÖŠ¼ÓČėĖ®µÄÄæµÄŹĒ_____”£
£Ø3£©ŌŚ½ųŠŠ½šŹōŠŌÖŹµÄŹµŃ鏱£¬Ä³Ķ¬Ń§½«Ģś·Ū¼ÓČėµ½Ź¢ÓŠĮņĖįĀĮŗĶĮņĖįĶµÄ»ģŗĻČÜŅŗÖŠ£¬³ä·Ö·“Ó¦ŗó¹żĀĖ£¬ĻņĀĖŌüÖŠµĪ¼ÓŃĪĖį£¬Ć»ÓŠĘųÅŻ²śÉś”£ŌņĀĖŅŗÖŠĖłŗ¬½šŹōĄė×ÓŅ»¶ØÓŠ_____ £ØĢīŠ“ŠņŗÅ£©”£
¢ŁAl3+¢ŚAl3+”¢Fe2+¢ŪAl3+”¢Fe3+¢ÜFe2+”¢Cu2+¢ŻAl3+”¢Fe2+”¢Cu2+
£Ø4£©ŹµŃéŹŅÓĆČēĶ¼×°ÖĆ½ųŠŠÄ£ÄāĮ¶ĢśµÄŹµŃ锣
¢Ł²£Į§¹ÜÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ_____”£
¢ŚŅŖÖ¤Ć÷ŹµŃéÖŠÓŠ¶žŃõ»ÆĢ¼Éś³É£¬»¹Šč½«×°ÖĆČēŗĪøĽų_____£æ
£Ø5£©ĀåŃōčļ“ØĻŲĖŲÓŠ”°ÖŠ¹śīā¶¼”±Ö®³Ę£¬čļ“ØīāŅµ¹«Ė¾Éś²śµÄīāĖįļ§£Ø£ØNH4£©2MoO4£©ŌŚŅ»¶ØĪĀ¶ČĻĀ·Ö½āÉś³É°±Ęų”¢Ė®ŗĶČżŃõ»Æīā”£Ēė¼ĘĖć98kgµÄīāĖįļ§£¬ĶźČ«·Ö½āæÉŅŌÖʵĆČżŃõ»Æīā¶ąÉŁĒ§æĖ_____£æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æČēĶ¼ŹĒA”¢BĮ½ĪļÖŹµÄČܽā¶ČĒśĻߣ¬ĻĀĮŠŠÅĻ¢ÖŠ£¬ÕżČ·µÄŹĒ
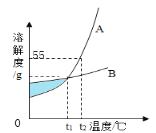
A. Ķ¼ÖŠŅõÓ°²æ·Ö±ķĆ÷A”¢BĮ½ČÜŅŗ¶¼ŹĒ±„ŗĶČÜŅŗ
B. t1”ꏱ£¬µČÖŹĮæµÄA”¢B±„ŗĶČÜŅŗÖŠČÜÖŹµÄÖŹĮæĻąµČ
C. t2”ꏱ£¬AĪļÖŹµÄ±„ŗĶČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹżĪŖ55%
D. t2”ꏱ£¬µČÖŹĮæµÄA”¢BĮ½±„ŗĶČÜŅŗ½µĪĀµ½t1”ꏱĪö³öČÜÖŹµÄÖŹĮæĻąĶ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø5·Ö£©ĖįÓźøųČĖĄąÉś»īŗĶÉē»į“ųĄ“ĮĖŃĻÖŲĪ£ŗ¦”£Ęū³µĪ²ĘųŹĒµ¼ÖĀĖįÓźµÄŌŅņÖ®Ņ»£¬ĪŖ¼õÉŁÓŠŗ¦ĘųĢåµÄÅÅ·Å£¬ČĖĆĒŌŚĘū³µĪ²Ęų¹ÜÉĻ°²×°”°“ß»Æ×Ŗ»ÆĘ÷”±£¬Ź¹Ī²ĘųÖŠµÄŅ»Ńõ»ÆĢ¼ŗĶŅ»Ńõ»ÆµŖ×Ŗ»ÆĪŖæÕĘųÖŠĢå»ż·ÖŹż×ī¶ąµÄĘųĢåŗĶCO2”£»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³ö×Ŗ»ÆµÄ»Æѧ·½³ĢŹ½ £»
£Ø2£©·“Ó¦ÖŠ£¬Ź§ŃõµÄĪļÖŹŹĒ £¬øĆĪļÖŹ¾ßÓŠ ŠŌ”££ØĢī”°»¹Ō”±»ņ”°Ńõ»Æ”±£©
£Ø3£©ÉĻŹö·“Ó¦²śÉśµÄ¶žŃõ»ÆĢ¼“óĮæÅÅ·Å»įµ¼ÖĀ £¬µĶĢ¼»·±£æĢ²»ČŻ»ŗ”£
£Ø4£©ŹµŃéŹŅÖŠČōŅŖ¼ģŃ鶞Ńõ»ÆĢ¼£¬»Æѧ·½³ĢŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com