
| 操作步骤 | 实验现象 | 结论或化学反应方程式 |
| 取少量样品置于试管中,加入足量稀硫酸,将试管用导管与澄清石灰水相连. | ①产生大量气体,使石灰水变浑浊. ②样品全部溶解,溶液呈蓝色. | ①样品中含有碳酸根(CO32-)离子 ②样品中含有铜(Cu2+)离子 |
| 在上述蓝色溶液中,插入一根洁净的铁丝. | ①铁丝表面缓缓产生少量气泡. ②片刻后铁丝表面出现红色物质. | ①Fe+H2SO4═H2↑+FeSO4 ②Fe+CuSO4═Cu+FeSO4 (均用方程式表示) |

| 装置A | 装置B | 装置C | 装置D | |
| 第一次 加热后 | 绿色粉末变黑色 | 白色粉末变蓝色 质量增加0.9g | 出现白色沉淀, 质量增加2.2g | 无明显变化 质量不改变 |
| 第二次 加热后 | 黑色粉末变红色 质量为6.4g | 无明显变化, 质量不改变 | 沉淀先增加后部分溶解; 质量增加 | 无明显变化 质量不改变 |
分析 此题为物质的推断题,完成此题,可以依据题干提供的信息,样品中加入稀硫酸有能使澄清石灰水变浑浊的气体产生,说明生成了二氧化碳,则样品中含有碳酸根离子,所得溶液与铁接触能生成红色固体,则有铜生成,说明溶液中含有铜离子,铁能与硫酸反应生成硫酸亚铁和氢气,能与硫酸铜反应生成硫酸亚铁和铜,无水硫酸铜遇水会变成蓝色,根据生成水的质量可以求得氢元素和氧元素的质量,根据红色粉末的质量可以求得铜的质量以及与铜结合的氧元素的质量,根据石灰水增加的量可以求得二氧化碳的质量,从而求得碳元素以及其中所含氧元素的质量.
解答 解:解:实验探究:样品中加入稀硫酸有能使澄清石灰水变浑浊的气体产生,说明生成了二氧化碳,则样品中含有碳酸根离子,所得溶液呈蓝色,说明含有铜离子,与铁接触能生成红色固体,则有铜生成,有气泡产生,则说明还有硫酸,铁能与硫酸反应生成硫酸亚铁和氢气,能与硫酸铜反应生成硫酸亚铁和铜,所以本题答案为:
| 操作步骤 | 实验现象 | 结论或化学反应方程式 |
| 取少量样品置于试管中,加入足量稀硫酸,将试管用导管与澄清石灰水相连. | ①产生大量气体,使石灰水变浑浊. ②样品全部溶解,溶液呈蓝色. | ①样品中含有 碳酸根(CO32- )离子 ②样品中含有 铜(Cu2+)离子 |
| 在上述蓝色溶液中,插入一根洁净的铁丝. | ①铁丝表面缓缓产生少量气泡. ②片刻后铁丝表面出现红色物质. | ①Fe+H2SO4═H2↑+FeSO4 ②Fe+CuSO4═Cu+FeSO4 (均用方程式表示) |
| 装置A | 装置B | 装置C | 装置D | |
| 第一次 加热后 | 绿色粉末变黑色 | 白色粉末变蓝色 质量增加0.9g | 出现白色沉淀, 质量增加2.2g | 无明显变化 质量不改变 |
| 第二次 加热后 | 黑色粉末变红色 质量为6.4g | 无明显变化, 质量不改变 | 沉淀先增加后部分溶解; 质量增加 | 无明显变化 质量不改变 |
| 操作步骤 | 实验现象 | 结论或化学反应方程式 |
| 取少量样品置于试管中,加入足量稀硫酸,将试管用导管与澄清石灰水相连. | ①产生大量气体,使石灰水变浑浊. ②样品全部溶解,溶液呈蓝色. | ①样品中含有 碳酸根(CO32- )离子 ②样品中含有 铜(Cu2+)离子 |
| 在上述蓝色溶液中,插入一根洁净的铁丝. | ①铁丝表面缓缓产生少量气泡. ②片刻后铁丝表面出现红色物质. | ①Fe+H2SO4═H2↑+FeSO4 ②Fe+CuSO4═Cu+FeSO4 (均用方程式表示) |
| 装置A | 装置B | 装置C | 装置D | |
| 第一次 加热后 | 绿色粉末变黑色 | 白色粉末变蓝色 质量增加0.9g | 出现白色沉淀, 质量增加2.2g | 无明显变化 质量不改变 |
| 第二次 加热后 | 黑色粉末变红色 质量为6.4g | 无明显变化, 质量不改变 | 沉淀先增加后部分溶解; 质量增加 | 无明显变化 质量不改变 |
点评 实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.


科目:初中化学 来源: 题型:解答题
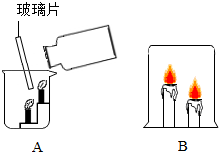 观察如图所示的实验,回答问题:
观察如图所示的实验,回答问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
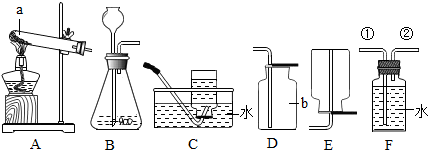
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | CaCl2溶液 | 稀盐酸 | 过量碳酸钙、过滤 |
| B | KOH溶液 | KCl | 适量稀盐酸 |
| C | NaCl溶液 | Na2CO3 | 适量硝酸钙溶液、过滤 |
| D | O2 | CO | 通过灼热的氧化铜 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
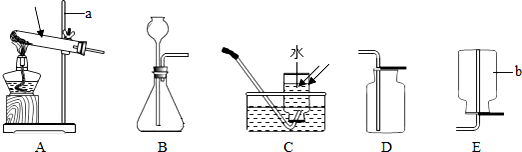
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com