
分析 (1)根据氧化铜和炭粉中只有氧化铜与稀硫酸反应,所以剩余的固体为炭粉;
(2)根据氧化铜的质量结合化学方程式计算生成硫酸铜的质量,进一步计算反应后所得溶液的溶质质量分数.
解答 解:(1)氧化铜和炭粉中只有氧化铜与稀硫酸反应,所以剩余的固体为炭粉;所以氧化铜的质量为10g-2g=8g,原粉末中氧化铜的质量分数为$\frac{8g}{10g}×100%$=80%;
(2)解:设得到的硫酸铜的质量为x.
CuO+H2SO4═CuSO4+H2O
80 160
8g x
$\frac{80}{8g}=\frac{160}{x}$
x=16g
硫酸铜的质量分数=$\frac{16g}{8g+192g}×$100%=8%
答:所得硫酸铜溶液的溶质的质量分数为8%.
故答案为:(1)80%;(2)8%.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出原混合物中氧化铜的质量是正确解答本题的前提和关键.


科目:初中化学 来源: 题型:填空题
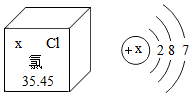 回答下列问题
回答下列问题查看答案和解析>>
科目:初中化学 来源: 题型:推断题
 如图所示A~G是初中化学中常见的物质(反应条件和部分产物已省略,“-”表示相互能反应,“→”表示转化关系),其中A是人体胃液中含有的酸,B与C的组成元素相同,D是一种红色粉末,F是相对分子质量最小的氧化物.请回答下列问题.
如图所示A~G是初中化学中常见的物质(反应条件和部分产物已省略,“-”表示相互能反应,“→”表示转化关系),其中A是人体胃液中含有的酸,B与C的组成元素相同,D是一种红色粉末,F是相对分子质量最小的氧化物.请回答下列问题.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 53:40 | B. | 53:19 | C. | 53:80 | D. | 53:28 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaHCO3是碱 | |
| B. | 该反应中四种物质都是盐 | |
| C. | 该反应不符合复分解反应发生的条件 | |
| D. | 析出晶体后剩余溶液中的溶质只有NH4Cl一种 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com