
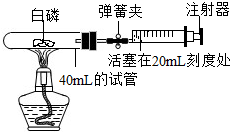
 为测定空气中氧气的含量,某兴趣小组的同学选用了40mL的试管作反应容器(如图)和量程体积足够大且润滑效果很好的针筒注射器,将足量的白磷放入试管后,用橡皮塞塞紧试管,并夹紧弹簧夹.用酒精灯加热白磷,燃烧结束后,等到试管冷却后松开弹簧夹,观察现象.
为测定空气中氧气的含量,某兴趣小组的同学选用了40mL的试管作反应容器(如图)和量程体积足够大且润滑效果很好的针筒注射器,将足量的白磷放入试管后,用橡皮塞塞紧试管,并夹紧弹簧夹.用酒精灯加热白磷,燃烧结束后,等到试管冷却后松开弹簧夹,观察现象.分析 (1)根据实验的原理分析实验前的操作.根据空气中氧气的体积分数计算分析;根据实验的原理及注意事项分析有关的操作对实验结果的影响;
(2)[提出猜想]根据空气的成分和固体的颜色判断淡黄色固体的来源;
[实验探究]根据在纯氧气中燃烧镁条只生成白色固体,在纯氮气中燃烧镁条只生成淡黄色色固体,可采取分别在纯氧气和纯氮气中燃烧镁条,观察现象的方法;
[实验结论]根据反应的反应物、生成物和反应条件书写方程式;
[反思与评价]根据镁可以在氮气中燃烧这一特殊性质分析回答.
解答 解:(1)①在该实验中利用白磷燃烧生成了五氧化二磷固体,消耗了试管内空气中氧气,根据体积的减小来测定空气中氧气的含量.要想实验成功,装置的气密性必需是好的.在正式开始实验前操作的主要目的是:检查装置的气密性.
②由于空气中氧气约占空气体积的$\frac{1}{5}$,所以试管内密封的40mL的空气中氧气约占8mL.所以,实验后,可以观察到针筒活塞会从原来的20mL刻度处慢慢向左移到约12mL处,内外压强相等.
③A.装置有点漏气,使测定的结果不准确;
B.白磷的量不足,不能将氧气全部消耗掉,使测定的结果偏小;
C.红磷、白磷都与氧气反应生成了五氧化二磷,对实验结果几乎没有影响.
(2)[提出猜想]空气中含有氮气,在空气中点燃镁条时,生成的白色固体物质中夹杂着少量的淡黄色固体,而氮化镁为淡黄色,所以淡黄色的固体可能是镁与空气中的氮气反应生成的.
[实验探究]由于在纯氧气中燃烧镁条只生成白色固体氧化镁,在纯氮气中燃烧镁条只生成淡黄色色固体氮化镁,分别在纯氧气和纯氮气中燃烧镁条,观察现象的方法.
[实验结论]镁和氧气在点燃的条件下燃烧生成氧化镁,方程式为:2Mg+O2 $\frac{\underline{\;点燃\;}}{\;}$2MgO;镁和氮气在点燃的条件下反应生成氮化镁,方程式:3Mg+N2 $\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
[反思与评价]一般情况下,氧气有助燃性,可以支持燃烧,而该题中显示镁在氮气中也可以燃烧,所以启示为:物质不一定只在氧气中才能燃烧或氮气通常不支持燃烧,但有时也能支持某些物质的燃烧.
答案:
(1)①检查装置气密性; C; AB
(2)[提出猜想]、氮气(或N2)
[实验探究]将点燃的镁条伸人充满氮气的集气瓶中,观察是否生成淡黄色的固体;
[实验结论]2Mg十O2$\frac{\underline{\;点燃\;}}{\;}$2MgO;3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2
[反思与评价]燃烧不一定要有氧气参加(其他合理答案均可).
点评 本题通过实验的创新,考查了我们分析问题的能力.在解答时,善于抓住题目的要点,才能使解答明晰不乱.


科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 二氧化碳气体能使燃着的木条熄灭,能熄灭火焰的气体一定是二氧化碳 | |
| B. | 单质只含有一种元素,含有一种元素的物质一定是单质 | |
| C. | 分子可以构成物质,但物质不一定都由分子构成 | |
| D. | 分子是由原子构成的,所以分子一定比原子大 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 第一次 | 第二次 | 第三次 | 第三次 | |
| 稀盐酸的用量 | 10g | 10g | 10g | 10g |
| 剩余固体的质量 | 6g | 4g | 2g | 2g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 选项 | 实验目的 | 所用试剂或方法 |
| A | 除去 CO2中的 O2 | 通过足量的灼热的铜网 |
| B | 实验室制取CO2 | 块状大理石和稀硫酸 |
| C | 除去 CO2中的 CO | 在氧气中点燃 |
| D | 鉴别O2与 CO | 伸入带火星的木条 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 鉴别的物质 | 鉴别的方法 |
| A | 水和过氧化氢溶液 | 加二氧化锰,观察是否有气泡 |
| B | 硫酸铜溶液与氯化钠溶液 | 观察颜色 |
| C | 二氧化碳与氮气 | 用燃着的木条 |
| D | 氯化钠与硝酸铵固体 | 加水测温度 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com