
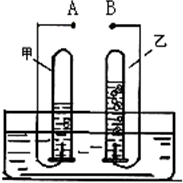
 如图是电解水的简易装置图,回答下列问题.
如图是电解水的简易装置图,回答下列问题.分析 根据已有的知识进行分析,电解水时与电源正极相连的试管内生成的是氧气,体积较小,与电源负极相连的试管内生成的是氢气,体积较大,在水中加入稀硫酸能增强水的导电性,检验氧气使用带火星的木条,该实验说明水是由氢元素和氧元素组成的.
解答 解:(1)水通电生成氢气和氧气,甲管内产生的气体较多,是氢气,乙管内的气体较少,是氧气,则电源B是正极;检验氧气使用带火星的木条,将带火星的木条伸进试管中,观察到木条复燃,故填:氢气;正;将带火星的木条伸进试管中,观察到木条复燃;水$\stackrel{通电}{→}$氢气+氧气;
(2)电解水生成氢气和氧气,氢气由氢元素组成,氧气有氧元素组成,该实验说明水是由氢元素和氧元素组成的,故填:氢元素和氧元素.
(3)电解水时,与正极相连的试管产生的是氧气,与负极相连的试管产生的是氢气,氢气和氧气的体积比约为2:1;因为氧气比氢气的溶解能力强,做该实验时,测得甲管和乙管中气体的体积比大于2:1.故填:2:1;氧气比氢气的溶解能力强.
点评 本题考查了电解水的知识,完成此题,可以依据已有的知识进行.


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:初中化学 来源: 题型:推断题
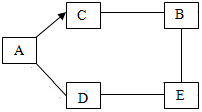 A~E为初中化学常见的五种物质,其类别各不相同,它们相互间的关系如图所示(“→”表示转化关系,“-”表示相互之间会反应).已知A是胃酸中含有的一种酸,C是氧化物,E的溶液呈蓝色,A、B、C、D、E的相对分子质量依次增大.(部分反应物、生成物及反应条件已略去).
A~E为初中化学常见的五种物质,其类别各不相同,它们相互间的关系如图所示(“→”表示转化关系,“-”表示相互之间会反应).已知A是胃酸中含有的一种酸,C是氧化物,E的溶液呈蓝色,A、B、C、D、E的相对分子质量依次增大.(部分反应物、生成物及反应条件已略去).查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 1 g酒精和1 g水混合后溶液的质量 | |
| B. | 1 g金属锌和1 g稀盐酸反应后溶液的质量 | |
| C. | 温度一定时1 g饱和硝酸钾溶液中加入1 g水后,所得溶液的质量 | |
| D. | 1 g氢氧化钠溶液和1 g稀硫酸混合后溶液的质量 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质的质量 | 甲 | 乙 | 丙 | 丁 |
| 反应前 | 25g | x | 5g | 5g |
| 反应后 | 8g | 23g | 5g | 8g |
| A. | 该反应是化合反应 | B. | x=9g | ||
| C. | 在该反应中,丙物质一定做催化剂 | D. | 在该反应中,甲丁的质量比为1:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com