
| ��Ӧʱ�� | t0 | t1 | t2 | t3 |
| �ձ�������/g | 161.4 | 161.2 | 161.0 | 161.0 |
���� �ⶨij���Ͻ�ĺ�������ʵ���Ͼ������ý��������ᷴӦ�����������������еļ��㣬Ҫ���������и��������ݣ��ó���ȷ�Ľ��ۣ�
��� �⣺��1����Ӧ��������������Ϊ11.4g+50.0g+100.0g-161.0g=0.4g��
��2����11.4g����������к���������Ϊx��
Fe+2HCl�TFeCl2+H2��
56 2
x 0.4g
$\frac{56}{2}$=$\frac{x}{0.4g}$����x=11.2g
�����������������������Ϊ$\frac{11.2g}{11.4g}$��100%=98.2%��
�𣺣�1����Ӧ��������������Ϊ0.4g����2�������������������������Ϊ98.2%��
���� ���⿼����ǻ�����д����ʵĺ����ļ��㣬��ɴ�����Ŀ��Ҫ����������漰���Ļ�ѧ��Ӧ�����������غ㶨�ɼ����ij���ʵ�������Ȼ����м��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ѡ�� | ʵ��Ŀ�� | �����Լ��� |
| A | ��ȥ��������Һ�е�����ͭ | �������������ۣ����� |
| B | Ӳˮ���� | ��л����� |
| C | ����¶���ڿ����е�����������Һ�Ƿ���� | ������ɫ��̪ |
| D | �����Ȼ��ƺ�����粒��� | ��ˮ�������ʯ����ĥ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  ������������Һ�м�������ˮϡ�� | |
| B�� |  ij�¶��£���ӽ����͵��Ȼ����Һ�м����Ȼ�茶��� | |
| C�� |  ���Ȼ���������Ļ����Һ�м����������������Һ | |
| D�� |  ��һ������ϡ�����м���������п�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
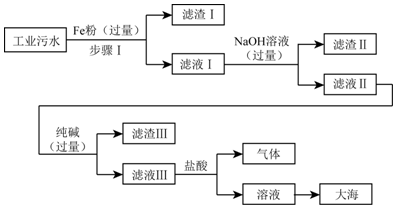
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
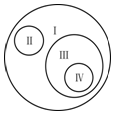 ���и�ѡ���Ĺ�ϵ������ͼ��ʾ�Ĺ�ϵ���ǣ�������
���и�ѡ���Ĺ�ϵ������ͼ��ʾ�Ĺ�ϵ���ǣ�������| ѡ�� | �� | �� | �� | �� |
| A | Ѫϸ�� | ��ϸ�� | ��ϸ�� | ѪС�� |
| B | ������ | θ | С�� | �� |
| C | ����ϵͳ | ���� | ����λ | ���� |
| D | Ӫ������ | ������ | ���� | ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com