
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | CO | CO2 | 将气体缓缓通过足量的澄清石灰水,并干燥 |
| B | CO2 | CO | 将混合气体点燃 |
| C | Cu | Zn | 加入过量的稀盐酸,过滤,洗涤,加热烘干 |
| D | FeCl2溶液 | CuCl2 | 加入过量的铁粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、CO2能与足量的澄清石灰水反应生成碳酸钙沉淀和水,CO不与足量的澄清石灰水反应,再进行干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、除去二氧化碳中的一氧化碳不能够点燃,这是因为当二氧化碳(不能燃烧、不能支持燃烧)大量存在时,少量的一氧化碳是不会燃烧的;故选项所采取的方法错误.
C、Zn能与稀盐酸反应生成氯化锌和氢气,铜不与稀盐酸反应,再过滤,洗涤,加热烘干,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、过量的铁粉能与CuCl2溶液反应生成氯化亚铁溶液和铜,再过滤,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:B.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
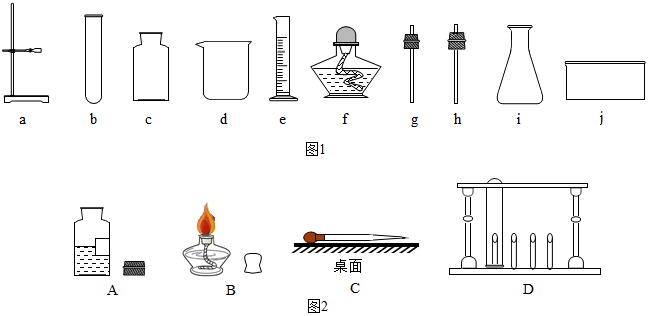
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NaOH H2SO4 BaCl2 | B. | NaOH CuSO4 NaCl | ||
| C. | HNO3 KNO3 K2SO4 | D. | Na2SO4 FeCl3 KCl |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 20℃ | 8%Na2CO3溶液 | 8%NaHCO3溶液 |
| pH | 10.6 | 8.0 |
| 溶解度 | 10℃ | 20℃ | 30℃ | 40℃ |
| Na2CO3 | 12.5g | 21.5g | 39.7g | 49.0g |
| NaHCO3 | 8.1g | 9.6g | 11.1g | 12.7g |
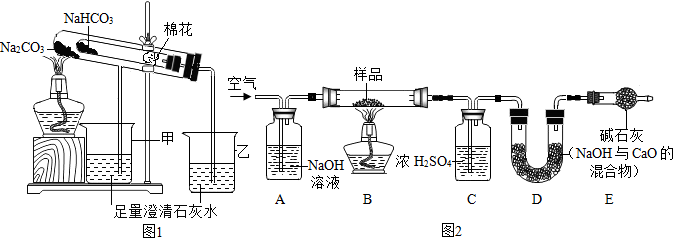
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 小军同学在探究质量守恒定律实验时,称取2.4g镁条在密闭的容器中点燃与充足的空气反应,其反应的化学方程式为2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.实验完毕后,称得所得固体的质量小于4.0g.
小军同学在探究质量守恒定律实验时,称取2.4g镁条在密闭的容器中点燃与充足的空气反应,其反应的化学方程式为2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.实验完毕后,称得所得固体的质量小于4.0g.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com