


分析 (1)根据配制溶液的步骤解答;
(2)根据配置溶液所需仪器解答;
(3)根据溶质质量=溶液质量×溶质质量分数解答;根据量筒的使用方法进行解答.
(4)根据固体的溶解度是指在一定温度下,某固体物质在100g水中达到饱和状态时所溶解的质量,根据固体物质的溶解度可以判断出在一定温度时形成的溶液是否饱和进行解答.
解答 解:
(1)配制溶液的步骤是:①计算,②称量,③量取,④溶解,⑤装瓶;
(2)配制过程除了用到图中所需仪器,还缺少玻璃棒;该仪器的作用是搅拌,加速溶解.
(3)配制50g溶质质量分数为5%的KCl溶液,需KCl的质量为0g×5%=2.5g;水的质量=50g-2.5g=47.5g,合47.5mL;俯视读数会导致量取的液体的体积偏小,从而导致所配制的溶液的溶质的质量分数偏大;
(4)由于氯化钾在20℃时的溶解度是34g,即100g水中最多溶解34g氯化钾,因此在20℃时在100g水中加入20g氯化钾,氯化钾会全部溶解,得到的A溶液是20℃不饱和溶液;又加入20g氯化钾,由于在100g水中最多溶解34g氯化钾,因此这20g氯化钾只能再溶解14g,所以形成的B溶液是20℃饱和溶液;升温至50℃,由于氯化钾在50℃时的溶解度是42.6g,因此后加入的氯化钾会全部溶解,而且形成的溶液C是50℃不饱和溶液,但又加入20g氯化钾,这20g氯化钾会再溶解2.6g,形成的溶液D是50℃饱和溶液,然后降温到20℃时,有晶体析出,形成溶液E是20℃饱和溶液.
故属于不饱和溶液的是AC,溶质的质量分数相同的是BE.
故答案为:
(1)溶解;(2)玻璃棒;搅拌,加速溶解; (3)47.5;偏大;(4)AC; BE.
点评 本题难度不大,主要考查了对固体溶解度概念的理解,从而培养学生对知识的应用能力和理解能力.熟练掌握配制溶液的步骤,仪器,溶质的质量分数计算是解答此题的基础和关键.


科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
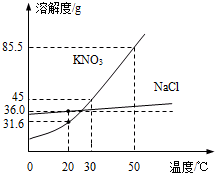 如图为NaCl、KNO3的溶解度曲线(水的密度约为1g/cm3).
如图为NaCl、KNO3的溶解度曲线(水的密度约为1g/cm3).查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 阴离子 阳离子 | OH- | NO3- | Cl- | SO42- | CO32- |
| H+ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 溶 | 不溶 | 不溶 |
| 实验目的 | 实验操作 | 现象 | 结论或化学方程式 |
| 除去碳酸钠 | 取少量该固体样品溶于水配成溶液,滴加适量的BaCl2溶液.充分反应后过滤 | 有白色沉淀生成 | 有关反应的化学方程式为 Na2CO3+BaCl2═BaCO3↓+2NaCl |
| 检验是否含有氢氧化钠 | 在滤液中滴加酚酞溶液 | 变红 | 该样品中含有氢氧化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在山林中遇火灾时,尽量向逆风方向奔跑,脱离火灾区 | |
| B. | 室内起火,立即打开所有门窗 | |
| C. | 有烟雾的地方,尽量贴近地面逃离 | |
| D. | 烟雾很大时,用湿毛巾捂住口鼻 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 增加私家车用量,提高生活质量 | |
| B. | 大力发展风能,减少火力发电 | |
| C. | 农作物秸秆多翻土还田,不露天焚烧 | |
| D. | 居民多用天然气,少用煤作燃料 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 0℃ | 10℃ | 20℃ | 30℃ | |
| Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 |

| 实验操作 | 实验现象 |
| ①取100g 20℃的水,加入35g碳酸钠固体,搅拌后,静置,取上层清液 ②利用装置二进行实验,连续5分钟向新制得的碳酸钠溶液中通入CO2 | 没有出现白色沉淀 |
| 实验操作 | 实验现象 |
| ①取100g热开水,加入35g碳酸钠固体,完全溶解,再降温至20℃,取上层清液 ②利用装置一和装置二分别进行实验,连续3分钟向新制得的碳酸钠溶液中通入CO2 | 装置一和装置二中的碳酸钠溶液中均出现白色沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com