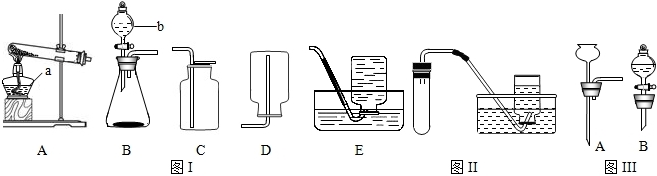
催化剂在生产、生活和科研中有着重要作用.实验室用分解过氧化氢制氧气,常用二氧化锰作催化剂.
【提出问题】其它物质能作过氧化氢分解的催化剂吗?
【猜想】甲同学认为CuO、Fe2O3可以代替MnO2,因为按物质的简单分类,CuO、Fe2O3、MnO2都属于______.
【设计实验】甲同学按下面步骤进行实验:
(1)在试管中加入5ml 5%的过氧化氢溶液,把带火星的木条伸入试管;
(2)用精密的天平准确称量0、5g Fe2O3红色粉末,并将其加入一试管中;
(3)在步骤(2)的试管中加入5ml 5%的过氧化氢溶液,将带火星的木条伸入试管;
(4)待步骤(3)的试管中没有气泡后,进行“某一操作”将固体洗净,干燥、称量,得红色固体的质量仍为0、5g.
【现象】甲同学观察到步骤(1)中的现象为______步骤(3)中带火星的木条复燃.
【反思】步骤(4)中“某一操作”为______乙同学认为步骤(4)后还应增加一个实验请写出该实验的步骤和现象______.
解:[猜想]CuO、Fe2O3、MnO2三种物质均为两种元素组成且含氧元素的氧化物;
[现象]常温下5mL5%的H2O2溶液分解缓慢,放出的氧气不足以使带火星的木条复燃;甲同学观察不到步骤①中伸入的带火星木条的复燃;
[反思]为证明氧化铁作为反应的催化剂,除以上检验加快反应速度外,还需要分离反应后剩余物中的氧化铁,以测定其质量不变.由于反应后氧化铁不溶于水故采用过滤的方式进行分离.
在确认质量不变时,还需要证明分离出来的固体氧化铁的化学性质是否发生了改变,通常采取再利用其做一次相同的催化作用实验;
故答案是:[猜想]氧化物;
[现象]带火星的木条没有复燃;
[反思]过滤;将得到的Fe2O3再次加入过氧化氢溶液中,过氧化氢溶液能较快产生氧气
分析:根据催化剂在反应中的特点,要想证明某种物质是催化剂,首先,加入这种物质前后反应速率是不是变化非常明显,其次反应前后这种物质的化学性质、质量均不变;如果该物质加入后,化学反应速率发生了明显改变,而自身在反应前后化学性质和质量都没有改变,可证明该物质为此反应的催化剂.
点评:此题考查了催化剂及催化作用的实验验证方法,利用实验分别进行了催化剂特性的验证,即化学反应前后催化剂质量没有增减,化学性质不会改变.



 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案