
| 实验步骤 | 实验现象 | 解释 |
| (1)将铁片、铜片分别投入到盛有稀盐酸的试管中. | 铁片的表面产生大量的气泡;铜片表面无现象; | 反应的化学方程式为:Fe+H2SO4=FeSO4+H2↑ |
| (2)将铜片投入到盛有AgNO3溶液的试管中. | 在铜片的表面覆盖了一层银白色物质,溶液呈蓝色. | 反应的化学方程式为:Cu+2AgNO3=2Ag+Cu(NO3)2 |
| 结论:Fe、Cu、Ag三种金属由强到弱的活动顺序为:Fe>Cu>Ag. | ||
分析 此题是金属活动性顺序的判断,通常可以通过金属与酸反应是否会产生气泡或者产生气泡的快慢来判断,也可以利用金属与盐溶液进行反应,看是否会发生置换反应生成新的金属来判断金属活动性的强弱.
解答 解:
由于三种金属Fe、Cu、Ag在金属活动顺序中铁排在氢的前面而铜和银排在氢的后面,所以这样我们可以分2步进行判断:首先是判断铁与铜的关系,可以用和酸反应的现在进行判断,铁在氢的前面可以与酸发生置换反应产生氢气,而铜不反应;第2步:判断铜和银的顺序,因为他们都在氢的后面所以可以利用与盐溶液的反应进行判断,实验2采用了铜与硝酸银反应,因为铜在银的前面所以可以把银置换出来.
故答案:
| 实验步骤 | 实验现象 | 实验解释 |
| (1)将铁片、铜片分别投入到盛有稀盐酸的试管中 | 铁片的表面产生大量的气泡,铜片表面无现象. | 反应的化学方程式: Fe+H2SO4=FeSO4+H2↑ |
| (2)将铜片投入到盛有AgNO3溶液的试管中 | 在铜片的表面覆盖一层银白色物质,溶液呈 蓝 色 | 反应的化学方程式: Cu+2AgNO3=2Ag+Cu(NO3)2 |
| 结论:Fe、Cu、Ag三种金属由强到弱的活动顺序为:Fe>Cu>Ag | ||
点评 本题是判断金属活动性强弱的,解题的时候是利用了金属活动性的2个应用,一是金属是否与酸反应,二是金属与盐溶液的反应,通过实验现象来判断.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:初中化学 来源: 题型:选择题
| A. | Zn | B. | Cu | C. | Zn、Cu | D. | Cu、Mg、Zn |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
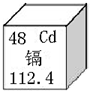 广西龙江河2012年1月15日出现重金属镉含量超标,1月26日污染水体进入下游柳江系统,给柳江流域造成了严重的水体污染,倍受社会各界关注.镉元素在元素周期表中的相关信息如图所示.下列说法中不正确的是( )
广西龙江河2012年1月15日出现重金属镉含量超标,1月26日污染水体进入下游柳江系统,给柳江流域造成了严重的水体污染,倍受社会各界关注.镉元素在元素周期表中的相关信息如图所示.下列说法中不正确的是( )| A. | 镉原子核内有48个质子 | B. | 镉元素的原子序数是48 | ||
| C. | 镉原子的相对质量是112.4g | D. | 镉属于金属元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
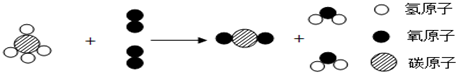
| A. | 有3种分子参加该反应 | |
| B. | 该反应属于分解反应 | |
| C. | 该反应的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O | |
| D. | 该反应属于化合反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验操作 | 实验现象 | 实验结论或化学方程式 |
| 步 骤 一 | 取样品,加水配制成溶液,并向其中滴加适量氯化钙溶液,充分反应后过滤 | 有白色沉淀生成 | 证明有碳酸钠,氢氧化钠已变质. 写出加入氯化钙溶液后发生反应的化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl. |
| 步 骤 二 | 取上述少量滤液于试管中,滴加无色酚酞溶液 | 酚酞溶液变 为红 色 | 证明有氢氧化钠, 结论:氢氧化钠部分变质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com