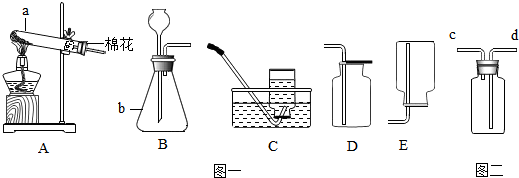
图1是几种实验室制取气体的发生装置与收集装置.
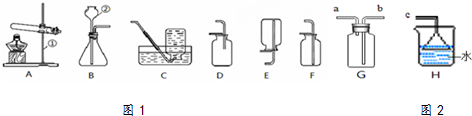
(1)写出有标号的仪器名称:①
②
(2)若用高锰酸钾制取氧气时,所选用的发生装置是
(填字母序号,下同),收集装置是C或
,反应的文字表达式为
(3)若用C装置收集氧气,正确的操作顺序为
(填编号).
a.将导管伸入集气瓶口,让气体进入瓶中
b.将装满水的集气瓶倒置在水槽中
c.当气体收集满时,用毛玻璃片盖住瓶口,将集气瓶移出水面正放置于桌面
(4)若用过氧化氢溶液和二氧化锰制取氧气,为了控制反应速率,获得平稳的气流,可用
(填一种仪器名称)代替B装置中的仪器②.实验结束后,若要分离出二氧化锰,可将残留物经过滤、洗涤、干燥.在过滤操作中玻璃棒的作用是
.若滤液仍浑浊,下列可能的原因有
(填编号)
①漏斗下端没有紧靠烧杯内壁 ②过滤器中的液面超过滤纸边缘
③滤纸没有紧贴漏斗内壁 ④玻璃棒没有靠在三层滤纸处,且将滤纸捅破
(5)氨气(NH
3)是一种无色有刺激性气味的气体,密度比空气小且极易溶于水.实验室用加热氯化铵和消石灰的固体混合物制取氨气.若选用图2中的G、H组合收集氨气,气体应从
(填“a”或“b”)端通入,另一端接H装置中的c,装置中漏斗的作用是
.
(6)实验室制取二氧化碳,一般选择的药品是
和稀盐酸.反应的文字表达式为
.为了检验二氧化碳,可选择G装置,瓶中先放适量的
(填试剂名称),然后将气体从
(填a或b)端通入.反应的文字表达式为
.若从图3甲乙丙中选择合适的装置制取二氧化碳,能达到“随开随用,随关随停”目的是
(填编号)
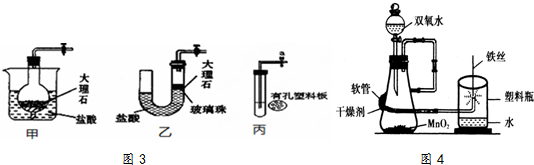
(7)图4是“铁丝在氧气中燃烧”实验的改进装置.实验时,打开分夜漏斗活塞,通入干燥氧气约10秒,引燃铁丝下端火柴杆,伸入塑料瓶内,并对准玻璃管口正上方,观察到的现象是:铁丝剧烈燃烧,
.
改进后装置具有的优点是
(填序号).
①氧气无需提前制备和收集,操作更方便
②塑料瓶代替集气瓶,防止集气瓶炸裂,更安全
③装置集氧气的制取、干燥和性质验证于一体,实验更优化
(8)小曹老师带领学生进行氧气性质实验时,发现“一同学不慎碰倒装满氧气的集气瓶,迅速扶起后,瓶中剩余的氧气仍能使带火星的木条复燃”;对此,小曹老师让该同学往集气瓶装入半瓶水,再用排水法收集
集气瓶的氧气,发现瓶中的氧气也能使带火星木条复燃.
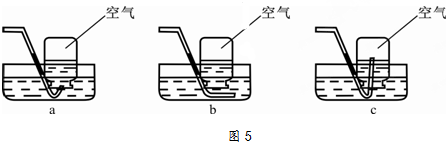
①用下列方案收集“
集气瓶的氧气”,其中最合理的是
(填字母).
②用排水法收集气体时,集气瓶中气体已收集满时的现象是
③空气中氧气的体积分数约为21%.本实验中,集气瓶内的氧气约占总体积的
,所以用“使带火星木条复燃”来检验集气瓶中充满氧气的方法不可靠.



 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案