
下图表示某些物质间转化关系。A、D为固体且组成元素相同,A为紫黑色;X、F为液体且组成元素相同,X具有消毒杀菌作用;E为产生温室效应的常见气体,Y是一种红色的金属。请回答下列问题:

(1)写出物质Y的化学式______;
(2)写出有关反应的化学方程式:②______;⑤_______。
(3)在反应③中,C物质的作用是_______。
(4)利用合成气在一定条件下可合成化工产品乙醇(C2H6O),请写出该化学反应方程式_______。
科目:初中化学 来源:江苏省扬州市2019届九年级下学期3月月考化学试卷 题型:单选题
下列物质的转化中,只有加入酸才能一步实现的是( )
A. Fe→FeSO4 B. CO2→H2CO3
C. CaCO3→CO2 D. CaCO3→CaCl2
查看答案和解析>>
科目:初中化学 来源:广东省广州市英文学校2019届九年级上学期期末考试化学试卷 题型:简答题
Mg(OH)2 被添加于塑料、橡胶等易燃物中,在受热分解时吸收热量并释放出水而起到阻燃作用,同时生成的氧化镁,化学性质稳定,不产生二次污染。
(1)写出Mg(OH)2 受热分解反应的化学方程式:_________________。
(2)实验室模拟制取Mg(OH)2 的一个实验是:一定温度下,往一定量氯化镁中加入氨水,生成Mg(OH)2 沉淀,再通过结晶、过滤,得到Mg(OH)2 晶体。为探究获得较高Mg(OH)2晶体转化率的条件,某研究小组进行下述对比实验,数据如下表:
实验 | 结晶温度/℃ | 结晶时间/min | 转化率/% |
a | 20 | 30 | 53.15 |
b | 40 | 30 | 84.12 |
c | 40 | 45 | 63.00 |
d | 60 | 60 | 62.20 |
①该小组研究的结晶条件是_____和_____。
②实验_____和_______(填序号)说明在其它条件相同的情况下,结晶时间相同时,温度越高,Mg(OH)2 转化率越高。
③实验b和c的目的是____。
④在上述四组实验中,最佳的结晶条件是____℃和_____min。
查看答案和解析>>
科目:初中化学 来源:广东省广州市英文学校2019届九年级上学期期末考试化学试卷 题型:单选题
浓硝酸和锌的反应的化学方程式为:Zn + 4HNO3 = Zn(NO3)2 + 2H2O + 2X↑,则X为
A.H2 B.NH3 C.NO D.NO2
查看答案和解析>>
科目:初中化学 来源:广东省广州市英文学校2019届九年级上学期期末考试化学试卷 题型:单选题
下列关于空气的说法中正确的是
A. 拉瓦锡用定量的方法研究了空气的成分 B. 空气中氮气体积分数约为21%
C. 空气质量指数越高说明空气质量越好 D. 洁净的空气是纯净物
查看答案和解析>>
科目:初中化学 来源:江苏省丹阳市2019届九年级上学期第二次月考化学试卷 题型:实验题
课本实验中,铁生锈需要较长的时间,某实验小组设计如下实验:

(1)写出甲试管中发生反应的化学方程式______;
(2)4分钟后观察:A处铁丝依然光亮,B处铁丝表面灰暗,D处铁丝依然光亮。该实验说明铁生锈主要与______和______有关;
(3)B、D处实验现象对比说明:决定铁生锈快慢的一个重要因素是______;
(4)请写出日常生活中防止铁生锈的一种措施______。
查看答案和解析>>
科目:初中化学 来源:江苏省丹阳市2019届九年级上学期第二次月考化学试卷 题型:多选题
有一种抗癌新药——西达本胺的化学式为C22H19FN4O2。下列关于西达本胺的说法正确的是
A. 一个西达本胺分子中共有48个原子
B. 西达本胺由碳、氢、氧、氮、氟五种元素组成
C. 西达本胺中碳元素和氮元素的质量比为11:2
D. 西达本胺各元素的质量分数中氧元素的质量分数最小
查看答案和解析>>
科目:初中化学 来源:安徽省亳州市2019届九年级下学期中考模拟化学试卷 题型:简答题
某化学兴趣小组同学为回收一块质量为40 g的铜锌合金中的铜,将该合金放人烧杯中,逐渐加入稀硫酸至不再产生气泡时,恰好用去稀硫酸100 g,烧杯内剩余固体27 g。请完成下列计算:
(1)40 g铜锌合金中锌的质量是________g 。
(2)计算所用稀硫酸中溶质的质量分数为_________。
查看答案和解析>>
科目:初中化学 来源:江苏省无锡市2019届九年级下学期3月月考化学试卷 题型:综合题
过氧化镁(MgO2)是一种镁精细化工产品。在医疗上可用来治疗消化不良、胃酸过多等疾病。在环境保护方面,过氧化镁可用来处理地下水污染的土壤。还可以用于牙膏,对牙齿有漂白和防过敏的作用。某化学兴趣小组对过氧化镁的性质和制备等进行了以下研究。
一.过氧化镁的性质
(1)过氧化镁(其中氧元素的化合价为____)是一种白色的粉末,其外观与物理性质与氧化镁相似。化学性质不够稳定,不溶于水,但逐渐的被分解放出氧气。
过氧化镁有强氧化性,常温下比较稳定,但是加热时会分解生成氧气和氧化镁。请下出该反应的化学方程式________。
(2)过氧化镁易溶于稀盐酸,发生反应:MgO2+2HCl=MgCl2+H2O2同时温度升高,说明该反应热量__________(填“放出”或“吸收”)。
二.过氧化镁的制备
下图是利用碱式碳酸镁(Mg2(OH)2CO3)和30%的过氧化氢溶液来制取过氧化镁。

(资料)①碱式碳酸镁与碳酸镁有相似的化学性质,能与稀盐酸反应产生二氧化碳②氧化镁与过氧化氢反应放出大量的热
(3)检测煅烧过程碱式碳酸镁完全分解的方法是_________(写出具体的操作和现象);上述生产过程加入稳定的剂的作用是________。
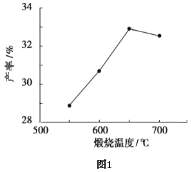
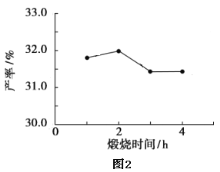
(4)用上述碱式碳酸镁在550、600、650及700℃下煅烧一定的时间生成氧化镁。用上述条件制备的氧化镁分别与30%双氧水反应合成过氧化镁产率(见图1和图2)。
碱式碳酸镁煅烧的温度适宜控制在________℃,煅烧的时间适宜控制在______h。
(5)结果在适宜的温度和时间下,碱式碳酸镁能完全分解,并且得到的氧化镁颗粒表面积最大,能与30%过氧化氢充分反应,所以产率高。推测700℃时,产率明显降低的可能的原因____。
三.过氧化镁产品纯度检测
在生产过程中,过氧化镁中常常含有少量的氧化镁杂质(其他杂质不考虑),以下是该小组进行纯度检测的实验装置和实验步骤。
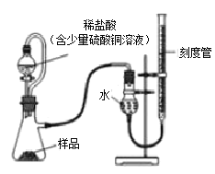
①检查装置气密性,装入药品(样品质量为0.7g),调节刻度管使左右两边液面相平,刻度管度数为10.0mL。
②打开分液漏斗开关,待瓶中无气泡产生时,关闭开关。
③再次调节刻度管使左右两边液面相平,刻度管度数为122mL。
(6)稀盐酸中放入的少量硫酸铜溶液目的是__________。
(7)根据上面实验数据计算样品中过氧化镁的质量分数__________(写出具体的计算过程,实验条件下O2密度为1.429g/L)。
(8)该小组同学所测得质量分数比实际结果偏大,你觉得可能的原因是(_______)
A 生成的氧气有少量溶于水 B 未等装置冷却到室温就开始读数
C 杂质与盐酸反应能产生少量的气体 D 滴入的稀盐酸占了一部分气体的体积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com