
分析 (1)根据高锰酸钾制取氧气的反应原理及实验装置要求分析解答;
(2)依据高锰酸钾制取氧气的反应物的状态和反应条件选择发生装置;据氧气的密度和溶解性选择收集装置解答;
(3)依据高锰酸钾制取氧气的反应原理书写方程式.
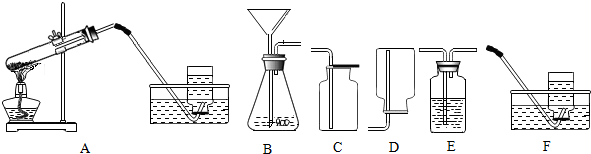
解答 解:(1)图中的四处错误是:试管口向上倾斜了,导管进入橡皮塞太长了,试管口没有棉花团,用酒精灯的焰心加热了;
(2)用高锰酸钾制取氧气需要加热,属于固体加热型,故选发生装置A;氧气的密度比空气大且不易溶于水,故可用向上排空气法或排水法收集.
欲制得干燥的O2气体,将你选择的装置顺序从左到右排列为AEC;
(3)高锰酸钾在加热下分解为锰酸钾、二氧化锰和氧气,方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
答案:(1)①试管口向上倾斜了;②导管进入橡皮塞太长了;③试管口没有棉花团;④用酒精灯的焰心加热了;
(2)A;C或F;AEC;
(3)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
点评 本题难度不大,掌握实验室制取氧气的注意事项是正确解答本题的关键.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 ”表示一个氧原子,则“
”表示一个氧原子,则“ ”表示的微粒是O2.
”表示的微粒是O2.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com