
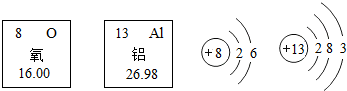
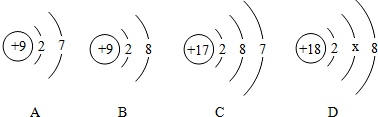
分析 (1)根据元素周期表中一小格的意义分析解答.
(2)根据化合物的化学式的写法来分析;
(3)根据微观粒子结构示意图来分析;
(4)根据元素周期表中每一横行元素从左向右排列时数字的变化及数字的意义来分析解答.
解答 解:(1)据图可以知道,铝元素的相对原子质量是26.98,故填:26.98.
(2)铝原子最外层有3个电子,易失去3个电子而显+3价,氟原子最外层有7个电子,易得到1个电子而显-1价,铝元素与氟元素组成的化合物的化学式是:AlF3;故答案为:AlF3;
(3)元素是具有相同核电荷数(即核内质子数)的一类原子的总称,故可知同种元素的原子具有相同的质子数;故填:AB;
最外层电子数决定元素的化学性质,AC最外层均为7个电子,易得到1个电子,化学性质相似;BD的最外层均为8个电子,均处于稳定结构,化学性质相似;故填:A和C;B和D;
原子的核内质子数=核外电子数;阳离子的核内质子数>核外电子数;阴离子的核内质子数<核外电子数,B所示粒子结构示意图中,质子数<电子数,属于阴离子;
故填:阴;
在原子中,质子数=核外电子数,所以X=18-2-8=8;故填:8;
(4)因周期表中元素符号前的数字为原子序数,也是原子的质子数,由元素周期表中每一横行元素从左向右排列可发现质子数在依次增大,故填:质子数递增.
点评 本题考查学生对元素周期表的认识,学生应明确元素周期表中的数字代表的意义并学会寻找规律是解答本题的关键.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 物质 | 不同温度下在水中溶解度(S/g) | 常温下在乙醇中的溶解度(S/g) | |||
| 0℃ | 10℃ | 20℃ | 30℃ | ||
| NaOH | 42 | 51 | 109 | 119 | 17.3 |
| Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 | <0.01 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 0.1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com