
【题目】下列关于物质的变化或物质的性质判断正确的是( )
A.生石灰变成熟石灰是物理变化
B.干冰升华是化学变化
C.蔗糖易溶于水是蔗糖的物理性质
D.铜能导电是铜的化学性质
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:初中化学 来源: 题型:
【题目】今年春季,我省部分地区雨水较少,出现了旱情,为了增强农作物的抗旱能力,小明建议父母施用适量的磷肥,下列化肥中属于磷肥的是( )
A.K2SO4 B.CO(NH2)2
C.Ca3(PO4)2 D.KNO3
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】自然界中的碳循环
碳是组成生物体的基本元素之一,也是组成煤、石油、天然气等的主要元素之一。自然界中的碳循环主要是通过CO2来实现的。如图是碳循环主要途径的模式图。

(1)结合图4,下列关于碳循环的认识正确的是(填序号 ) 。
A.有机物和无机物可以相互转化
B.碳循环过程只涉及到化学变化
C.碳循环过程中,各元素的化合价都不变
D.燃烧过程中能量的转化形式是化学能转化为热能和光能
(2)用化学方程式表示图 4碳循环中的下列变化:①动物体内的葡萄糖在酶的作用下发生缓慢氧化,生成二氧化碳和水 。②消耗二氧化碳的一种方式 。
(3)从化学的视角看物质
目前,人们对二氧化碳的评论褒贬不一。若以“二氧化碳的利与弊”做为论题,你的观点是
,请列举有力的证据论证你的观点。
要求:①论据简洁、论证充分。②同一论据举出一个事例即可。③字数在100字以内。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】绍兴市获得2015年度全省“五水共治”工作优秀市并被授予大禹鼎,“五水共治”是指治污水、防洪水、排涝水、保供水、抓节水,还社会一个蓝天碧水,为百姓创造美好的生活环境。
某化工厂流程会产生澄清废水,其中可能含有的离子是Ag+、Cu2+、Cl﹣、NO3﹣,已知:白色的沉淀Fe(OH)2在空气中会迅速转化为红褐色的Fe(OH)3。
(1)取少量废水,加入过量稀盐酸,产生白色沉淀;再加入过量氢氧化钠溶液,产生蓝色沉淀。该废水中含有的金属离子是 。
(2)兴趣小组设计了一个除去该废水中原有金属离子的实验方案,部分流程如图所示。

操作I的名称是 ,单质A是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下物质:①氧气②蒸馏水③新鲜的空气④铜片⑤高锰酸钾(填序号)
(1)属于混合物的有 ,(2)属于纯净物的有 ,
(3)属于单质的有 ,(4)属于化合物的有 ,
(5)属于氧化物的有 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生活中处处有化学,在实际生活中下列物质的用途与其化学性质有关的是( )
A.干冰用作制冷剂 B.金刚石用作玻璃刀
C.氮气用作食品防腐剂 D.石墨用作电池的电极
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组在研究溶液的酸碱性时发现,Mg与NH4Cl溶液(酸性)反应有气泡产生。为确定气体的成分,进行下列实验探究:
【提出猜想】气体可能是HCl,NH3,H2中的一种或几种。
【查阅资料】NH3和HCl常温下会生成NH4Cl固体;NH3、HCl极易溶于水。
【实验探究】
为确定是否含有HCl,将气体通入含有硝酸的硝酸银溶液中,观察到_________,说明该气体中无HCl。
为了探究NH3和H2是否存在,又设计如下实验装置(假设每步反应均完全):
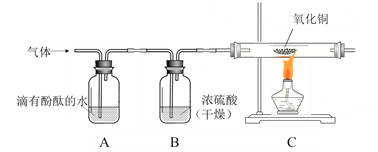
Ⅰ. A中观察到_________,证明有NH3;
Ⅱ. B中玻璃管内观察到__________,证明有H2;
【实验结论】Mg与NH4Cl溶液反应产生的气体是NH3和H2。
【实验反思】综合以上信息和实验结论,有同学认为无需单独检验HCl,就能证明HCl不存在。请评价这种说法是否合理并阐述理由_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属镁是一种重要的金属。小明在做镁带燃烧实验时,发现从实验室中取出来的镁条表面呈灰黑色,这灰黑色物质是什么呢?是氧化镁吗?小明想了一下,很快就把它否定了,他的理由是 。小明通过查阅资料灰黑色固体为碱式碳酸镁。
【查阅资料】1.碱式碳酸镁有多种组成。如Mg2(OH)2CO3、Mg4(OH)2(CO3)3、等,可以表示为xMgCO3·yMg(OH)2(x、y都是正整数)。
2.MgCO3![]() MgO +CO2 ↑ ;Mg(OH)2
MgO +CO2 ↑ ;Mg(OH)2![]() MgO +H2O
MgO +H2O
3.碱式碳酸镁能与盐酸反应生成氯化镁、二氧化碳和水。
Ⅰ.确定镁带表面碱式碳酸镁的成分
小明同学为确定镁带表面碱式碳酸镁的组成,设计如图所示的实验:
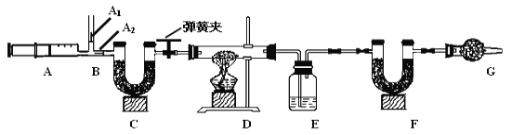
图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭。
【实验步骤】
①按图组装好仪器后, ;
②称取灰黑色样品,并将其放入硬质玻璃管中;
③打开弹簧夹,反复推拉注射器;
④称量E、F的质量,E的质量为87.6g,U型管F的质量为74.7g;
⑤关闭弹簧夹,加热D处试管直到反应不再进行;
⑥打开弹簧夹,再次反复缓缓推拉注射器;
⑦再次称量E、F的质量,E的质量为89.4g,U型管F的质量为87.9g。
【问题讨论】
(1)补充好实验步骤 ,E中所装药品是 ;
(2)C、F、G中装有碱石灰(CaO与NaOH的固体混合物),则C的作用是 ,若没有G装置,则测定的x的值会 (填“偏大”、“偏小”、“无影响”);
(3)步骤⑥目的是 ;
(4)根据上述实验数据,推算该碱式碳酸镁的化学式为 。
Ⅱ.测定镁带样品纯度

【问题讨论】
(5)装置B的作用是 ,装置C的作用是 ;
(6)称取1.0g镁带样品与足量浓盐酸充分反应后,收集到的氢气的体积为0.448 L(已知该实验条件下氢气的密度为0.089g/L),计算镁带样品纯度(写出计算过程,2分)
(7)有同学认为用这种方法测定的结果一定偏大,原因是 ;
(8)小江同学认为测定产物中CO2的质量(即反应前后装置②的质量差)也可测定样品中单质镁的纯度。但利用上述实验装置测得CO2的质量并计算样品的纯度,结果偏低,你认为原因可能是 。(填序号)
①浓盐酸易挥发,产生的氯化氢气体被装置
②二氧化碳气体逸出时带出的水蒸气在装置B中冷凝而被吸收
③装置A、B内空气中的二氧化碳被装置B吸收
④实验结束时烧瓶中残留二氧化碳
⑤气体从氢氧化钠溶液中逸出时带走部分水蒸气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com