


分析 (1)①根据实验室用浓盐酸和石灰石制取的二氧化碳中混有氯化氢、水蒸气,硝酸银会与盐酸反应,浓硫酸有吸水性,除去水蒸气需要放在最后,二氧化碳的密度比空气大进行分析;
②根据碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
③根据浓盐酸具有挥发性进行分析;
(2)①根据铁和水蒸气在高温的条件下生成四氧化三铁和氢气进行分析;
②根据D装置中减少的质量就是氧化铜中氧元素的质量,装置C2的质量增加的质量就是生成水的质量,C1装置是除去反应中的水蒸气,装置D中仍有少量黑色固体,说明氧化铜没有完全反应进行分析;
③根据氧化铜和氢气在加热的条件下生成铜和水,碱石灰有吸水性进行分析.
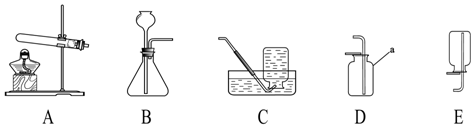
解答 解:(1)①实验室用浓盐酸和石灰石制取的二氧化碳中混有氯化氢、水蒸气,硝酸银会与盐酸反应,浓硫酸有吸水性,除去水蒸气需要放在最后,二氧化碳的密度比空气大,所以所选仪器的连接顺序应为ACBE;
②碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
③浓盐酸具有挥发性,所以装置D中出现异常现象的原因:浓盐酸具有挥发性,导致制取的二氧化碳中混有氯化氢气体,混合气通过澄清石灰水时,盐酸会先与氢氧化钙反应,导致二氧化碳不能与氢氧化钙反应,二氧化碳也不会与氯化钙反应,所以澄清石灰水不变浑浊;
(2)①铁和水蒸气在高温的条件下生成四氧化三铁和氢气,化学方程式为:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
②A、D装置中减少的质量就是氧化铜中氧元素的质量,装置D的质量减少mg,则样品中含有氧化铜为:$\frac{mg}{\frac{16}{80}}$=5mg,故A正确;
B、碱石灰有吸水性,装置C2的质量增加的质量就是生成水的质量,水中氧元素的质量为:ng×$\frac{16}{18}$=$\frac{8}{9}$ng,所以样品中含有氧化铜$\frac{\frac{8ng}{9}}{\frac{16}{80}}$=$\frac{40ng}{9}$,故B错误;
C、C1装置是除去反应中的水蒸气,若不连接装置C1,则通过装置C2质量的增加的质量偏大,计算出的氧化铜质量偏大,故C正确;
D、装置D中仍有少量黑色固体,说明氧化铜没有完全反应,所以则通过装置D质量的减少计算出的氧化铜质量偏小,故D错误;
故选:AC;
③氧化铜和氢气在加热的条件下生成铜和水,碱石灰有吸水性,所以仪器D中减少的是氧化铜中的氧元素的质量;而仪器C2中增加的是反应生成的水的质量.
故答案为:(1)①ACBE;
②CaCO3+2HCl=CaCl2+H2O+CO2↑;
③浓盐酸具有挥发性,导致制取的二氧化碳中混有氯化氢气体,混合气通过澄清石灰水时,盐酸会先与氢氧化钙反应,导致二氧化碳不能与氢氧化钙反应,二氧化碳也不会与氯化钙反应,所以澄清石灰水不变浑浊;
(2)①3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2;
②AC;
③氧化铜中的氧元素,反应生成的水.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 原子种类 | 质子数 | 中子数 | 核外电子数 | 相对原子质量 |
| 氢 | 1 | 0 | 1 | 1 |
| 碳 | 6 | 6 | 6 | 12 |
| 氧 | 8 | 8 | 8 | 16 |
| 钠 | 11 | 12 | 11 | 23 |
| 铁 | 26 | 30 | 26 | 56 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | S+O2$\frac{\underline{\;点燃\;}}{\;}$ SO2 | B. | 2CO+O2$\frac{\underline{\;点燃\;}}{\;}$2CO2 | ||
| C. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$ 2H2O | D. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氯化钾 | B. | 尿素 | C. | 硫酸钾 | D. | 过磷酸钙 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧气能支持燃烧,可作燃料 | |
| B. | 氧气能跟所有物质发生氧化反应 | |
| C. | 水中的生物能依靠易溶于水的氧气而生存 | |
| D. | 氧气可以变成液态或固态雪花状物质 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
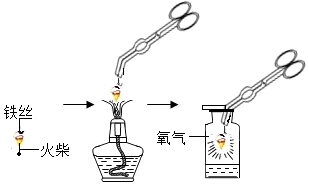 氧气是初中化学中的常见气体,请结合有关知识回答下列问题:
氧气是初中化学中的常见气体,请结合有关知识回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com