
分析 CO和CO2混合气体通过足量灼热的氧化铜,CO与氧化铜发生反应生成铜和二氧化碳,而使气体质量增加;因此,利用充分反应后气体增加的量,根据反应的化学方程式可计算出参加反应的CO的质量.
解答 解:反应后气体的质量比反应前增加了32%,则增加的是氧化铜氧元素的质量,故氧化铜中氧元素的质量为:5g×32%=1.6g
设混合气体中CO的质量为x
CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 气体的质量增加
28 44 44-28=16
x 1.6g
$\frac{28}{16}=\frac{x}{1.6g}$
x=2.8g
则混合气体中CO的质量分数为$\frac{2.8g}{5g}×$100%=56%
答:原混合气体中CO的质量分数是56%.
点评 根据反应前后气体物质的质量变化,利用化学方程式的气体差量进行参加反应气体的计算,可使复杂的计算得以简化.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
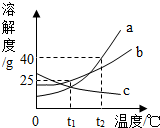 如图,a、b、c三种固体物质的溶解度变化如图所示.
如图,a、b、c三种固体物质的溶解度变化如图所示.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
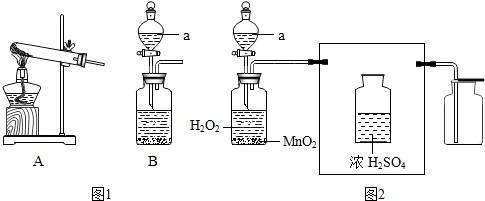
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com