
【题目】某兴趣小组的同学对一包久置的生石灰(CaO)干燥剂产生了好奇,于是他们对这包干燥剂的成分展开了探究。
【提出问题】这包干燥剂是否变质,成分是什么?
【猜想假设】猜想一:全部是CaO; 猜想二:是CaO和Ca(OH)2的混合物;
猜想三:全部是Ca(OH)2; 猜想四:是Ca(OH)2和CaCO3的混合物。
【实验探究】(1)取部分该干燥剂于试管中,加水无放热现象,说明干燥剂中不含 。
(2)继续向试管中滴加足量稀盐酸,有气泡出现,说明这包干燥剂中含有 。
(3)为了进一步确定这包干燥剂中有无其他成分,小组同学设计了以下二种方案。
另取部分干燥剂于烧杯中,加水并搅拌,静置后取上层清液于3支试管中。请你参与实验,并填写表中的空白:
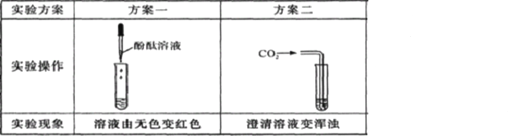
写出方案二发生的化学反应方程式 。
【实验结论】通过以上实验探究,得出猜想 成立。
【拓展迁移】小组同学反思生石灰干燥剂变质原因,认识到实验室保存氧化钙应注意 。
【答案】⑴CaO或氧化钙
⑵CaCO3或碳酸钙。 Ca(OH)2+CO2==CaCO3↓+H2O
四 密封保存 (其他合理答案均可)
【解析】分析:首先要仔细阅读题中所给的信息,抓到题干中的相关信息.对于第一小题(1)在该干燥剂中加入书水没有发热现象,根据知识点生石灰与水变熟石灰放出大量热可知一定不含生石灰;第二小题探究(2)中加足量酸有气泡推断肯定含有碳酸盐那么可以判断出该干燥剂中一定含有了碳酸钙;第三小题根据三个方案的实验探究,首先第一个实验方案指示剂的颜色变化肯定含有碱性物质,第二个方案通入二氧化碳变浑浊说明含有氢氧化钙;第三个方案也更说明含有氢氧化钙更由此猜想四是正确的.通过科学实验探究我们应该反思:在化学实验室保存氢氧化钙是一定不能漏置在空气中,否则会与空气中的二氧化碳发生反应而变质.
解答:(1)加水没有发热现象根据氧化钙(生石灰)的特性可以判断一定没有生石灰存在.因此正确答案:CaO或氧化钙;
(2)加入足量的酸有气泡产生说明该干燥剂中一定含有 CaCO3,但不能判断是否一定还有氢氧化钙,因Ca(OH)2遇到酸不会有气泡产生所以不能判定一定含有氢氧化钙.故正确答案:CaCO3或碳酸钙;
(3)常用澄清的石灰水来检验二氧化碳的存在,它会变浑浊是白色沉淀物碳酸钙,对于沉淀一定要加沉淀号↓;此为是水.所以化学方程式:Ca(OH)2+CO2═CaCO3↓+H2O;由以上实验探究得出猜想一,二,三都不可能有这几种情况的存在故答案:四; 由于氢氧化钙会和空气中的二氧化碳发生反应而变质所以要避免与空气接触即正确答案:密封保存


科目:初中化学 来源: 题型:
【题目】小明和小英要验证一块石头是否含碳酸钙。
(1)小明说:“只要取一小块石头放在烧杯中,再在石块上倒入盐酸,发现有大量气泡产生,就能证明石块含有碳酸钙。”小英说:“在石块上倒盐酸,产生的大量气泡是盐酸挥发而成的。”小英的说法对吗?_______(填“对”或“不对”)。
(2)小明和小英带着问题请教王老师,在王老师的指导下,进行了下列实验探究,其实验过程如下:①取一小块石块置于烧杯中,滴加盐酸后,发现产生了无色无味气体;②在老师的指导下,取①中的溶液检验,石块中含有钙元素;③他们又设计了如图所示的实验装置,在实验中观察到广口瓶中有浑浊现象产生。
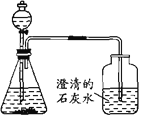
在上述实验中,他们进行的是_______实验研究(填“定性”或“定量”)。
(3)假若称取10.0 g石块与足量的稀盐酸反应(杂质不与盐酸反应),并用饱和石灰水吸收,得到的沉淀经适当处理后得干燥固体7.5 g。计算:
①石块中含碳酸钙的质量分数_______________;
②已知CO2在标准状况下的密度为1.98 g/L,则生成标准状况下CO2气体的体积为______________毫升?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下图回答相关问题:
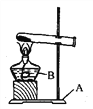
(1)若试管中的药品是碳酸氢铵,观察到_______色固体逐渐_______,试管口有_______,且有_______气味的气体产生,如将产生气体通入澄清石灰水,将会看到_______。
(2)由此实验可知,碳酸氢铵贮存时应注意______________。
(3)若试管中的药品为铜绿,则观察到_______色固体逐渐变为_______,是因为生成了______________(填物质名称)。
(4)加热过程中试管破裂,可能的原因是:
①________________________________________________________。
②________________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小明、小方两位同学分别按如图所示装置进行了探究活动。
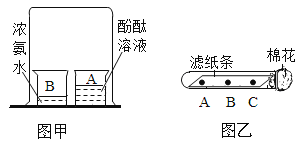
关于上述探究活动有下列说法:①A烧杯中的无色酚酞试液变红色;②B烧杯中的试液不变色;③滤纸上的酚酞试液由外向里依次变红;④两位同学的实验都能得出分子是不断运动的结论;⑤无色酚酞溶液变色属于物理变化;⑥一个氨气分子具有刺激性气味。以上说法正确的是( )
A.①② B.③④ C.⑤⑥ D.①②③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属.
(1)地壳中含量最高的金属元素是__________.
(2)根据图示金属应用实例推断,金属具有的物理性质有___________________.

(3)日常使用的金属材料多数属于合金.表中列出了一些常见合金的主要成分和性能.
合金 | 合金的主要性能 | 主要成分及纯金属的性能 |
焊锡 | 熔点183℃ | 锡:熔点232℃;铅:熔点327℃ |
硬铝 | 强度和硬度好 | 铝、铜、镁等.硬度小,质软 |
不锈钢 | 抗腐蚀性好 | 铁、铬、镍等.纯铁抗腐蚀性能不如不锈钢 |
由上表推断,与组成合金的纯金属相比,合金的优点一般有________________.
①强度更低②硬度更高 ③熔点更高 ④抗腐蚀性更好
(4)人们每年要从金属矿物资源中提取数以亿吨计的金属.根据所学化学知识,按要 求写出两个生成金属的化学方程式:
①___________________________________________________(置换反应);
②___________________________________________________(分解反应) .
(5)2008年奥运会主运动场“鸟巢”使用了大量的钢铁.钢铁与_____________直接接触容易生锈造成损失,在钢铁表面涂油、刷漆等,都能防止钢铁生锈.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小丁通过学习知道,电解水时生成氢气、氧气的体积比为2:1,但他在实验开始时发现氢气和氧气的体积比略大于2:1。你认为该现象的合理解释是 ( )
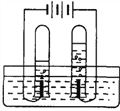
A. 要敢于质疑书本知识,书上的数据本来就是错的
B. 氧气比氢气更易溶于水
C. 生成的氧气有一部分跑到了试管外
D. 氧气的密度比氢气大得多,更难从水中升到水面上
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下是一些常见物质问互相转化的关系图。已知反应①的条件是加热,反应②的条件是点燃,反应③不需要其它条件,反应④的条件是通电。
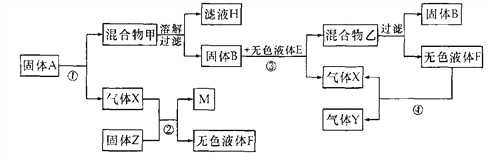
(1)将固体A充分加热至不再产生气体,滤液H中所含有的物质有:_____________ (写化学式)过滤操作中使用到的玻璃仪器是______________________。
(2)固体B的为____________,它在与无色液体E的反应中起____________作用。
(3)写出反应①③④的文字表达式:
①____________________________________________________
③____________________________________________________
④____________________________________________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属与生活密切相关.阅读下列材料,回答问题.
材料一:合金是人类应用最早的金属材料.如青铜、黄铜(铜、锌合金,外观与黄金极其相似).合金比组成它的纯金属有更多优良性能,如抗腐蚀性好、硬度大等.
材料二:锂是银白色固体、质软、自然界密度最小的金属,跟水反应生成氢气和氢氧化锂.在电池、航空航天等领域有广泛的用途.
材料三:锂的原子结构示意图及他与钠在周期表中的信息如图所示.

(1)用黄铜片在纯铜片上刻画_____(填“会”或“不会”)留下痕迹.一块由黄铜冒充的黄金,检验其真伪发生反应的化学方程式为_____.
(2)金属锂的物理性质有_____;金属锂与钠有相似的化学性质,其原因是_____.氢氧化锂与二氧化碳反应的化学方程式为_____,在航天舱内如果要吸收航天员呼出的二氧化碳气体,用氢氧化锂比氢氧化钠更理想,其原因是_____.
(3)将一定量的铜和锌同时投入硝酸银溶液,充分反应后过滤,得到固体和蓝色滤液.由此,能否判断金属活动性:Zn>Cu>Ag,说明理由_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氯化钠有着广泛用途,不但是重要的调味品,又是重要的工业原料。
(1)通过晾晒海水或煮盐井水、盐湖水等均可得到含有较多杂质的氯化钠晶体——粗盐,这种方法属于__________变化(填“物理”或“化学”)。粗盐经过__________、过滤、__________可得到初步提纯。
(2)钠与氯气反应时,每个钠原子失去______个电子形成钠离子(Na+),每个氯原子得到______个电子形成氯离子(Cl-),Na+与Cl-由于静电作用而结合成NaCl。
(3)氯气和氢氧化钠反应生成氯化钠、次氯酸钠和水(Cl2+2NaOH=NaCl+NaClO+H2O),工业上常用氯气和石灰水反应制漂白粉,其反应原理与上述反应相同,请写出制漂白粉的化学方程式__________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com