
分析 (1)根据原子得失电子情况与化合价关系分析.(2)根据阴极附近阳离子得电子,阳极附近阴离子 失去电子分析;(3)电解熔融Al2O3可制得Al单质和氧气.
解答 解:(1)在电解水的实验中,与直流电源正极相连的一极(阳极)可收集到O2,与直流电源负极相连的一极(阴极)可收集到H2,所以阴极附近阳离子(H+)得电子,元素的化合价降低,阳极附近阴离子(OH-)失去电子,元素的化合价降升高;
(2)电解已经在高温下融化的NaCl液体可制得Na单质和氯气中,钠离子在阴极上得电子形成钠原子,钠原子聚集成Na单质;
(3)根据上述原理,电解熔融Al2O3可制得Al单质和氧气,反应方程式为2Al2O3(熔融)$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑,
故答案为:(1)得;降低;(2)Na单质(3)2Al2O3(熔融)$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑.
点评 本题考查点解实验中电极上发生的变化,侧重于学生的分析能力的考查,注意从元素化合价的角度分析,难度较大.


科目:初中化学 来源: 题型:选择题
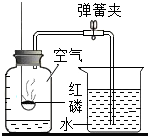 如图所示装置可用于测定空气中氧气的含量,会使测量结果偏大的操作是( )
如图所示装置可用于测定空气中氧气的含量,会使测量结果偏大的操作是( )| A. | ③ | B. | ①③ | C. | ②④ | D. | ①② |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 自然界中的水都不是纯水 | B. | 水是由氢气和氧气组成的 | ||
| C. | 加入洗涤剂的水可以溶解油污 | D. | 可以用煮沸的方法鉴别软水与硬水 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用5%的双氧水制氧气是为了避免反应过快 | |
| B. | 用36.5%的浓盐酸制得的二氧化碳更纯净 | |
| C. | 用98%浓硫酸检测金属的活动顺序更准确 | |
| D. | 用100%纯净水电解才能准确测定水的组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com