
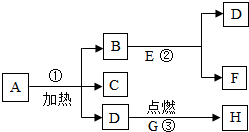
 A、B…H八种物质,有如图所示关系:其中D能使带火星的木条复燃,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变:
A、B…H八种物质,有如图所示关系:其中D能使带火星的木条复燃,H是一种能使澄清石灰水变浑浊的气体,在②的反应前后B的质量和化学性质都不改变:分析 根据D能使带火星的木条复燃,故D为氧气;结合图框,A受热分解生成三种物质且生成氧气,根据实验室制氧气的三种方法可知A为高锰酸钾,分解生成锰酸钾、二氧化锰和氧气;根据H是一种能使澄清石灰水变浑浊的气体,故H为二氧化碳,G是一种黑色的固体且能在氧气中燃烧生成二氧化碳,故G为碳.在②的反应前后B的质量和化学性质都不改变,故B二氧化锰,则C为锰酸钾;反应②是E和二氧化锰在常温下反应生成氧气,故E为双氧水,则F为水.代入检验.
解答 解:根据D能使带火星的木条复燃,故D为氧气;结合图框,A受热分解生成三种物质且生成氧气,根据实验室制氧气的三种方法可知A为高锰酸钾,分解生成锰酸钾、二氧化锰和氧气;根据H是一种能使澄清石灰水变浑浊的气体,故H为二氧化碳,G是一种黑色的固体且能在氧气中燃烧生成二氧化碳,故G为碳.在②的反应前后B的质量和化学性质都不改变,故B二氧化锰,则C为锰酸钾;反应②是E和二氧化锰在常温下反应生成氧气,故E为双氧水,则F为水.代入检验,符合题意.
(1)由上述分析可知:物质C为锰酸钾,E为双氧水;故其化学式分别为:K2MnO4;H2O2;
(2)反应为高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,文字表达式为:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;
(3)反应①为高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,符合“一变多”的特点,为分解反应;反应②双氧水和二氧化锰在常温下反应生成氧气,符合“一变多”的特点,为分解反应;反应③碳燃烧生成二氧化碳,符合“多变一”的特点,为化合反应;故上述关系中属于分解反应的是①②.
故答案为:
(1)K2MnO4; H2O2;(2)高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;(3)①②
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.解答本题的关键是熟练掌握常见物质的性质及现象.


 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验序号 | 氯酸钾质量 | 其他物质质量 | 待测数据 |
| ① | 1.2g | / | |
| ② | 1.2g | Fe2O3 0.5g | |
| ③ | 1.2g | MnO2 0.5g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在化合物中金属元素显正价,非金属元素一定显负价 | |
| B. | 镁和红磷都属于单质 | |
| C. | 矿泉水和蒸馏水都属于纯净物 | |
| D. | 氧气、氮气、氢气、铁都是由分子构成的 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 只含硫元素 | B. | 一定含氧元素 | ||
| C. | 一定含硫、氧、氢元素 | D. | 一定含硫、氢元素,可能含氧元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
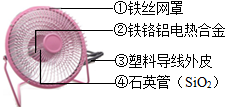 金属材料是工农业生产和人们生活离不开的材料之一,人类每年要从自然界获取大量的金属材料资源.根据对金属和金属材料的认识,回答:
金属材料是工农业生产和人们生活离不开的材料之一,人类每年要从自然界获取大量的金属材料资源.根据对金属和金属材料的认识,回答:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com