

| A. | ④ | B. | ③④ | C. | ①④ | D. | ②③④ |
分析 ①根据粗盐提纯中难溶性杂质的去除的操作步骤是溶解、过滤、蒸发进行分析;
②根据溶解、过滤、蒸发操作中的玻璃棒的作用进行分析;
③根据配制一定质量分数的溶液的步骤:计算、称量(量取)、溶解,根据各操作注意事项进行分析;
④根据乙实验中,若①所用的烧杯内壁沾有水,会造成溶剂的质量偏大进行分析.
解答 解:①粗盐中难溶性杂质的去除的操作步骤是溶解、过滤、蒸发,即步骤是①④⑤,其中去除杂质的关键一步是过滤(把不溶于液体的固体与液体分离的一种方法),故①错误;
②甲实验各步操作中,溶解时玻璃棒的作用是搅拌,能够加快粗盐的溶解速率;过滤时玻璃棒的作用是引流;蒸发时玻璃棒的作用是搅拌,防止液体飞溅;玻璃棒的作用不相同,故②错误;
③配制一定质量分数的溶液的步骤:计算、称量(量取)、溶解,乙实验按照②③①的步骤进行操作,③中量取的水的体积偏小,则配制的溶液浓度偏大,故③正确;
④乙实验中,若①所用的烧杯内壁沾有水,会造成溶剂的质量偏大,则会导致配制的溶液浓度偏小,故④正确.
故选:B.
点评 本题难度不大,掌握粗盐提纯的步骤与注意事项、配制一定质量分数的溶液的步骤与注意事项是正确解答本题的关键.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水是一种常见的溶剂 | B. | 长期饮用蒸馏水不利于人体健康 | ||
| C. | 过滤能除去天然水中所有的杂质 | D. | 明矾可促进水中悬浮杂质的沉降 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氮气、氯酸钾、钢 | B. | 氧气、水、澄清石灰水 | ||
| C. | 可燃冰、干冰、冰水混合物 | D. | 石墨、熟石灰、石油 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| Fe(OH)3 | Cu(OH)2 | |
| 开始沉淀的pH | 1.9 | 4.7 |
| 沉淀完全的pH | 3.2 | 6.7 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
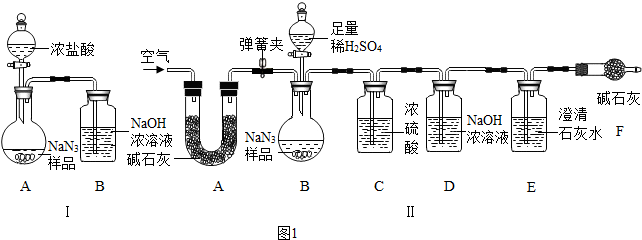
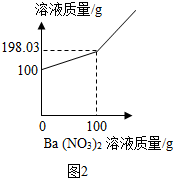
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铜具有良好的导电性 | B. | 铁锅炒菜是利用铁的导热性 | ||
| C. | 焊锡(锡铅合金)的熔点比锡高 | D. | 铁在潮湿的空气中容易生锈 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com