
钠及其化合物是中学化学学习和研究的重要内容.
(1)如图是钠的原子结构示意图.下列说法不正确的是 .
a.钠属于金属元素 b.钠原子的质子数为11
c.钠离子的符号为Na+ d.钠在化学反应中易得到电子
(2)钠与水反应生成氢氧化钠和氢气,化学方程式为 ;小苏打受热分解成碳酸钠、二氧化碳和水,化学方程式为 .
(3)在Cu(NO3)2、Al(NO3)3和AgNO3的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体上滴加稀硫酸时有气泡产生.则反应后所得溶液中含有的金属离子有 A ;反应后溶液的质量比原混合溶液的质量 (填“大”或“小”);写出有关反应的一个化学方程式 .
(4)某工厂利用废铁屑和废硫酸起反应来制取硫酸亚铁.现有废硫酸49t(H2SO的质量分数为10%),与足量的废铁屑起反应,可生产硫酸亚铁的质量是多少?


【考点】金属的化学性质;原子结构示意图与离子结构示意图;反应类型的判定;书写化学方程式、文字表达式、电离方程式;根据化学反应方程式的计算.
【专题】金属与金属材料.
【分析】(1)根据钠原子的结构图进行分析;
(2)根据反应物、生成物以及反应条件书写化学方程式;
(3)依据活动性强的金属可以把活动性弱的金属从其盐溶液中置换出来,所以铁可以置换出铜与银但不能置换出铝,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气泡产生,此现象说明Fe过量没有反应完,所以原混合溶液中的Cu(NO3)2、AgNO3全部被置换生成Cu、Ag和Fe(NO3)2溶液,A1(NO3)3不反应,再利用反应时金属的原子量可对溶液质量的改变进行分析,确定溶液质量的变化;
(4)根据化学方程式找出硫酸和硫酸亚铁的质量比,再根据硫酸的质量通过方程式可计算出生成硫酸亚铁的质量.
【解答】解:(1)a、由图片信息可知为钠元素的相关信息,则元素名称为钠,带有金字旁,属于金属元素,故说法正确;
b、由图片信息可知,钠原子的质子数为11,故说法正确;
c、钠元素的最外层有1个电子,容易失去电子,形成钠离子Na+,故说法正确;
d、钠元素的最外层有1个电子,容易失去电子,故故说法错误.
故选:d;
(2)钠和水反应生成氢氧化钠和氢气,化学方程式为:2Na+2H2O=2NaOH+H2↑;小苏打(NaHCO3)受热分解成碳酸钠、水和二氧化碳,反应的化学方程式为:2NaHCO3
 Na2CO3+H2O+CO2↑.
Na2CO3+H2O+CO2↑.
故填:2Na+2H2O=2NaOH+H2↑;2NaHCO3
 Na2CO3+H2O+CO2↑.
Na2CO3+H2O+CO2↑.
(3)混合溶液中的Cu(NO3)2、AgNO3与铁发生置换反应,得到Cu、Ag,铁粉过量,所以滤出固体中含Fe;反应后的溶液中即滤液不再含的Cu(NO3)2、AgNO3,而是含有生成的Fe(NO3)2;由于Al(NO3)3不与Fe发生反应,所以滤液中还含有Al(NO3)3;
依据该置换反应的过程是Fe十2AgNO3=Fe(NO3) 2+2Ag;Fe+Cu(NO3) 2=Fe(NO3) 2+Cu反应的铁与铜银的原子量关系可知:该两个反应发生时“铁”置换银与铜时反应的铁都小于生成的“铜和银”,故溶液质量减小;该过程中共发生两个化学反应:铁和硝酸铜的置换反应,铁和硝酸银的置换反应;
故答案为:Al3+ 和Fe2+;小;Fe+Cu(NO3)2=Fe(NO3)2+Cu(或Fe+2AgNO3=Fe(NO3)2+2Ag).
(4)设可生产硫酸亚铁的质量为x.
Fe+H2SO4 =FeSO4 +H2↑
98 152
49 t×10% x
根据:
 =
=

解得x=7.6 t
答:可生产硫酸亚铁7.6 t.
【点评】此题是对金属活动性顺序的考查,解题的关键是掌握金属活动性顺序表的意义,只有这样才能做出正确的判断.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:初中化学 来源: 题型:
下列图像能正确反映对应变化关系的是( )
| A | B | C | D |
| 一定温度下,向不饱和硝酸钾溶液中加入硝酸钾 | 向一定量NaOH溶液中加入稀H2SO4 | 向一定量铁粉和铜粉的混合物中加入硫酸铜溶液 | 向相等质量的锌粉和铁粉中,分别加入质量分数相同的稀盐酸 |
|
|
|
|
|
查看答案和解析>>
科目:初中化学 来源: 题型:
有四种物质的溶液①Ba(OH)2 ②Na2SO4 ③HNO3 ④FeCl3,不用其它试剂就可以将它们逐一鉴别出来,其正确的顺序是( )
A.①③④② B.④③②① C.①④②③ D.④①②③
查看答案和解析>>
科目:初中化学 来源: 题型:
以下对生活中的一些事实解释不合理的是( )
A.铁栏杆上涂油漆主要是为了防止生锈
B.不能用铁桶配置波尔多液(硫酸铜溶液与石灰乳混合),是因为硫酸铜会腐蚀铁桶。
C.海水晒盐没有把海水直接蒸发干,目的是防止海水中的可溶性杂质随氯化
钠一起结晶析出
D.实验室探究工业炼铁的反应原理的实验中,先通入CO是为了得到较纯净的铁
查看答案和解析>>
科目:初中化学 来源: 题型:
下列离子组能在溶液中大量共存的是( )
A.NO3﹣ H+ Na+ OH﹣ B.K+ SO42﹣ Na+ NO3﹣
C.Cl﹣ K+ SO42﹣ Ba2+ D.Ca2+ Cl﹣ CO32﹣ K+
查看答案和解析>>
科目:初中化学 来源: 题型:
下列四个图像分别对应四种操作(或治疗)过程,其中正确的是
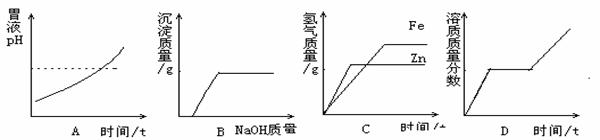
A、用胃舒平[主要成分Al(OH)3]治疗胃酸过多时pH情况。
B.向氯化铁的溶液中加入氢氧化钠溶液直至过量。
C.常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应。
D.将一定质量的硝酸钾不饱和溶液恒温蒸发水分,直到有晶体析出。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com