
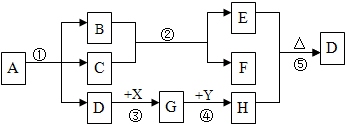
分析 根据A是绿色粉末,分解会生成三种物质,所以A就是碱式碳酸铜,碱式碳酸铜分解会生成氧化铜、水和二氧化碳,G是蓝色溶液,所以G中有铜离子,X为常见的稀盐酸,所以D就是氧化铜,G就是氯化铜,二氧化碳和水光合作用会生成有机物葡萄糖和氧气,E是氧气,H是铜,铜和氧气混合加热会生成氧化铜,氯化铜和Y会生成铜,所以Y是比铜活泼的金属,将推出的各种物质进行验证即可.
解答 解:(1)D是CuO;E是O2;X是HCl.
故填:CuO;O2;HCl.
(2)反应①中,碱式碳酸铜分解生成氧化铜、水和二氧化碳,反应的化学方程式为:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑;
反应②中,二氧化碳和水在一定条件下反应生成葡萄糖和氧气,反应的化学方程式为:6CO2+6H2O$→_{叶绿素}^{光}$C6H12O6+6O2.
故填:Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑;6CO2+6H2O$→_{叶绿素}^{光}$C6H12O6+6O2.
(3)反应③中,氧化铜和稀盐酸反应生成氯化铜和水,反应的化学方程式为:CuO+2HCl=CuCl2+H2O.
故填:CuO+2HCl=CuCl2+H2O.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


 小题狂做系列答案
小题狂做系列答案科目:初中化学 来源: 题型:实验探究题
| 猜想 | 主要操作 | 主要现象 | 实验结论 |
| 猜想一 | 打磨R丝,并将其插入到硫酸铜溶液中 | R丝表面覆盖了一层红色的物质 | 猜想一不成立(填“成立”或“不成立”) |
| 猜想二 | 打磨粗细相同的R丝、铝丝、铜丝,分别将它们插入到体积相同、溶质质量分数也相同的稀硫酸中 | ①R丝表面产生气泡缓慢,溶液由无色逐渐变成蓝色 ②铝丝表面产生气泡较快 ③铜丝表面没有气泡产生 | 猜想二成立. R与稀硫酸反应的化学方程式为 R+H2SO4=RSO4+H2↑ |
| 猜想三 | 将铝丝插入到RSO4溶液中 | 无明显现象 | 猜想三成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 物质 | K2CO3 | K2SO4 | KMnO4 |
| 溶解度/g | 111 | 11.1 | 6.34 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 金属用途广泛,其结构、性质等是化学的重要研究内容.
金属用途广泛,其结构、性质等是化学的重要研究内容.| 实验步骤 | 现象 | 有关反应的化学方程式 |
| 取少量固体B,滴加稀盐酸 | 有气泡产生 | Zn+2HCl═ZnCl2+H2↑ |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com