
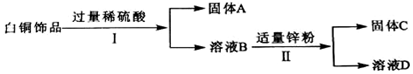
分析 根据金属能与酸反应的排在氢前面,不能与酸反应的排在氢的后面,活泼的金属能把不活泼的金属从盐溶液中置换出来分析金属活动性的顺序及反应过程中发生的反应并分析溶液中的成分.
解答 解:根据金属的活泼性顺序:铜在氢的后面与酸不反应,可知白铜饰品中加入过量的稀硫酸,镍可以与硫酸反应,已知溶液B中含有一种二价金属硫酸盐,故反应的化学方程式为:Ni+H2SO4=NiSO4+H2↑;溶液B为硫酸镍和稀硫酸的混合物,再加入适量的锌粉,因为溶液D中只有一种溶质,所以是锌与硫酸反应生成硫酸锌和氢气,锌与硫酸镍反应生成硫酸锌和镍,说明锌比镍活泼,所以
(1)由以上分析可知:固体A的化学式为Cu,过程Ⅱ中的实验操作名称是过滤,所用到的玻璃仪器有玻璃棒、烧杯和漏斗;
(2)过程Ⅰ中的反应是镍和硫酸反应生成硫酸镍和氢气,化学方程式为:Ni+H2SO4=NiSO4+H2↑;
(3)Cu、Ni、Zn的金属活动性由强到弱的顺序是:Zn>Ni>Cu.
故答案为:(1)Cu,过滤,漏斗;
(2)Ni+H2SO4=NiSO4+H2↑;
(3)Zn>Ni>Cu.
点评 本题以实验设计流程的形式让学生去利用金属活动性顺序表解决有关金属化学性质的问题,有一定的难度,解题的关键是熟练运用金属活动性的顺序意义.


科目:初中化学 来源: 题型:选择题
| A. | 20℃时KNO3的溶解度、80℃时KNO3的溶解度 | |
| B. | 30℃时:NaCl不饱和溶液的质量分数、NaCl饱和溶液的质量分数 | |
| C. | 10g铝与10%盐酸反应生成H2的速率,10 g镁与10%盐酸反应生成H2的速率、 | |
| D. | NaOH溶于水后溶液的温度、NH4NO3溶于水后溶液的温度 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用托盘天平称量2.53g的食盐固体 | |
| B. | 启用闲置的地窖前先进行灯火实验 | |
| C. | 过滤时用玻璃棒搅拌以加快速度 | |
| D. | 用品尝的方法区分实验室中的食盐和蔗糖 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硝酸铵 | B. | 生石灰 | C. | 浓硫酸 | D. | 氢氧化钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com