
【题目】氨气是一种无色有刺激性气味的气体,密度比空气_____,是氮肥工业的重要原料。
(1)实验室常用浓氨水和氢氧化钠固体混合制取少量氨气,产生氨气的原因有:
①氢氧化钠固体溶于水放热,促使氨水分解生成氨气,化学方程式为:_____![]() NH3↑+H2O。
NH3↑+H2O。
②氢氧化钠固体溶于水放热,使氨气在水中的_____,有利于氨气逸出。
(2)某化学兴趣小组为探究分子的运动情况,在玻璃管两端同时放入蘸有溶液的棉花,做了图1所示实验,发现在玻璃管内形成了白色烟环(成分为氯化铵)且偏向蘸有浓盐酸的棉花一端。
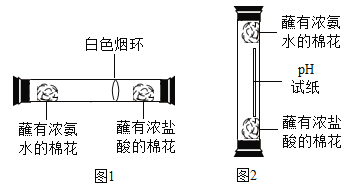
①白色烟环偏向蘸有浓盐酸的棉花一端的原因是_____;
②写出该反应的化学方程式:_____。
(3)为了获得更好的视觉效果,该小组同学设计了图2所示实验。
(实验步骤)从玻璃管顶部将蘸有浓盐酸的棉花投入底部(过程中棉花不接触管壁),pH试纸迅速变为红色;再将蘸有浓氨水的棉花固定在玻璃管顶部,用摄像机记录实验现象。
(查阅资料)图3所示是本实验所用的pH试纸的显色范围。

(现象分析)图4所示是摄像机记录下来的pH试纸每15s的显色情况。
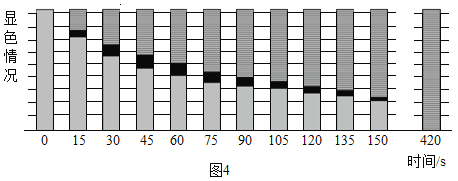
420s时,pH试纸全部变为绿色,白烟大部分沉降至量筒底部。图4中,75s时pH试纸从上至下的颜色依次为绿色、_____和_____。
(拓展探究)上述实验中,若上下棉花颠倒,即玻璃管底部是蘸有浓氨水的棉花,顶部是蘸有浓盐酸的棉花,则pH试纸几乎直接变为绿色,玻璃管内迅速充满白烟,解释产生这种现象的原因:_____。
(4)氯化铵是一种常见的氮肥。某氯化铵化肥的含氮量经测定是25.2%,已知杂质不含氮元素,则此化肥中氯化铵的质量分数为_____(计算结果保留一位小数)。
【答案】小 NH3H2O![]() H2O+NH3↑ 溶解度减小 相同条件下,氨分子比氯化氢分子运动的快 NH3+HCl═NH4Cl 黄色 红色 氯化氢气体的密度比空气大,氨气的密度比空气小,两种气体更快反应 96.3%
H2O+NH3↑ 溶解度减小 相同条件下,氨分子比氯化氢分子运动的快 NH3+HCl═NH4Cl 黄色 红色 氯化氢气体的密度比空气大,氨气的密度比空气小,两种气体更快反应 96.3%
【解析】
解:氨气是一种无色有刺激性气味的气体,密度比空气小,是氮肥工业的重要原料;
(1)①氢氧化钠固体溶于水放热,促使氨水分解生成氨气,即氨水在受热的条件下生成氨气和水;②氢氧化钠固体溶于水放热,使氨气在水中的溶解度减小,有利于氨气逸出;
(2))①相对分子质量越大,分子的运动速率越慢,相对分子质量越小,分子的运动速率越快,氨气的相对分子质量小于氯化氢的相对分子质量,所以氨分子的运动速率大于氯化氢分子的运动速率,所以生成的白色烟环偏向蘸有浓盐酸的棉花一端;
②氨气和氯化氢气体反应生成氯化铵,反应的化学方程式为:NH3+HCl═NH4Cl;
(3)420s时,pH试纸全部变为绿色,白烟大部分沉降至量筒底部。图4中,75s时pH试纸从上至下的颜色依次为绿色、黄色和红色;拓展探究中,产生这种现象的原因:氯化氢气体的密度比空气大,氨气的密度比空气小,两种气体更快反应;
(4)25.2%÷![]() ×100%=96.3%。
×100%=96.3%。


科目:初中化学 来源: 题型:
【题目】某工厂废液中含有AgNO3、Cu(NO3)2两种溶液,取部分废液于烧杯中,加入一定量锌粉,测定所得溶液中某溶质质量与时间的关系如下图,同时得到以下结论,其中说法错误的是( )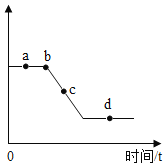
A.图中纵坐标表示Cu(NO3)2的质量
B.在a点表示的溶液中加稀盐酸,一定有白色沉淀产生
C.c点时烧杯中有两种金属单质,d点时烧杯中有三种金属单质
D.完全反应后过滤,向滤渣中加稀盐酸,一定无气泡产生
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下面的实验仪器省去了固定装置,请根据要求回答问题:
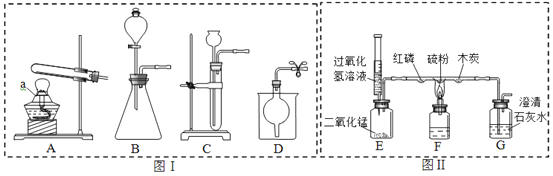
(1)仪器a的名称______,其用途是______。
(2)图Ⅰ中可用于实验室制取少量CO2且能控制反应的发生和停止的装置是______,反应的化学方程式为______。
(3)图Ⅱ是一套创新实验装置,可用于多种不同实验。
①检查这套装置的气密性时,先在G导管末端连接橡皮管,夹紧止水夹,______,若______,则装置不漏气。
②实验时,先推入过氧化氢溶液,E中的反应现象______,加热时硫粉处的现象为______,此时G中的石灰水变浑浊,反应的化学方程式为______。
③E与图Ⅰ中的______有相同的作用,其操作上的优点是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】碳酸亚铁(FeCO3)可用于制作补铁药物,以下是用硫铁矿烧渣(主要成分为 Fe2O3、SiO2 等)为原料制备碳酸亚铁的生产流程示意图:
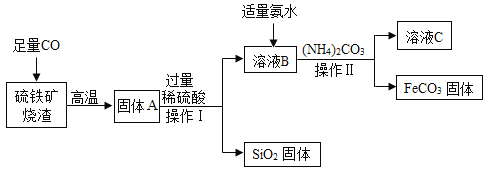
[资料]40℃以上时,(NH4)2CO3 易分解
(1)操作 I 所用到的玻璃仪器有烧杯、玻璃棒和 _____。
(2)加入(NH4)2CO3 后,该反应必须控制的条件是 _____。
(3)从溶液 C 中可回收一种化工产品——(NH4)2SO4,请写出它的一种用途: _____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶液具有广泛的用途。
(1)一种或几种物质分散到另一种物质里,形成_____,叫做溶液。
(2)在两支试管里各加入1~2小粒高锰酸钾,然后分别加入5mL水、5mL汽油,振荡,观察到的现象是_____。这说明,同一物质在不同溶剂中的溶解性是不同的。
(3)某注射用药液的配制方法如下:
①把1.0g药品溶于水形成4.0mL溶液a;
②取0.1mL溶液a,加水稀释至1.0ml,得溶液b;
③取0.1mL溶液b,加水稀释至1.0ml,得溶液c;
④取0.2mL溶液c,加水稀释至1.0ml,得溶液d;由于在整个配制过程中药液很稀,其密度可近似看做1g/cm3。经计算,溶液d中溶质的质量分数为_____,1.0g该药品可配制溶液d的体积是_____mL。
(4)20℃时,氢氧化钠,碳酸钠分别在水、酒精中的溶解度如表所示,20℃,将20g氢氧化钠分别投入100g水、100g酒精中,能和氢氧化钠形成饱和溶液的是_____(填“水”或“酒精”);用玻璃管向氢氧化钠的酒精溶液中不断吹气,观察到_____,证明二氧化碳与氢氧化钠发生了反应。
溶剂 | 20℃时的溶解度/g | |
氢氧化钠 | 碳酸钠 | |
水 | 109 | 21.8 |
酒精 | 17.3 | <0.01 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据下列装置图,回答有关问题:
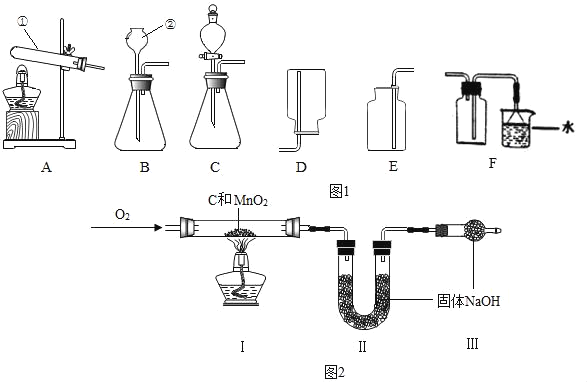
(1)写出图1中标号仪器的名称:①_____,②_____。
(2)实验室用高锰酸钾制氧气时发现水槽中水变红了,可能原因是_____。
(3)用双氧水制取氧气的化学方程式是_____,为得到平稳的氧气选用的发生装置是_____。用如图2装置从废旧干电池中回收MnO2并测定其含量,假设各步均完全反应,下列数据中可以计算样品中MnO2的含量的是_____。
a.反应前后氧气发生装置的质量
b.反应前后装置Ⅰ中固体的质量
c.反应前后装置Ⅱ中固体的质量
d.反应前后装置Ⅲ中固体的质量
(4)已知氨气是一种无色有刺激性气味的气体,密度比空气小,极易溶于水。实验室加热氯化铵和熟石灰固体制取并收集一瓶氨气,最佳的实验装置组合是_____。
(5)你认为实验室制取气体的反应,共同点是_____。
a.需要加热 b.反应物中没有气体参加
c.需要催化剂 d.反应物中必须含有要制取物质的元素。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】溶液与人们的生活息息相关。
(1)下列少量物质分别放入水中,充分搅拌,可以得到溶液的是_____(填字母)。
A 高锰酸钾 B 汽油 C 面粉 D 碘单质
(2)氢氧化钠、碳酸钠分别在水、酒精中的溶解度如表所示
氢氧化钠 | 碳酸钠 | ||||
20℃ | 40℃ | 20℃ | 40℃ | ||
水 | 109g | 129g | 21.8g | 49g | |
酒精 | 17.3g | 40g | 不溶 | 不溶 | |

①上述图象表示_____(填“氢氧化钠”或“碳酸钠”)的溶解度曲线。
②20℃时,氢氧化钠的溶解度_____(填“大于”或“小于”)碳酸钠的溶解度。
③40℃时,分别将50gNaOH分别投入到100g水和100g酒精中,能形成饱和溶液的是_____(选填“水”或“酒精”),再将适量CO2通入所得NaOH的酒精溶液中,观察到的现象为_____,反应的化学方程式为:_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】试管实验节约药品操作简便现象明显,是课堂教学中研究物质性质与变化的重要方法与手段。下列是初中化学中常见的几组实验:
(1)分别取少量氧化铁粉末和一根生锈铁钉于A、B两支试管中,分别加入等质量的稀盐酸并在酒精灯上微热,观察到两试管中溶液均变黄色,而B试管中还有大量气泡产生。两试管中均发生反应的方程式为_____________,B试管中所得溶液的溶质成分是_____________,一段时间后A试管没有明显变化,B试管中溶液颜色变成浅绿色,这可能是____________之间发生了进一步的反应。
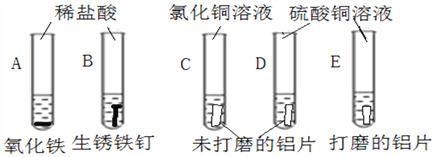
(2)将两片大小、形状相同的未打磨的铝片分别放入C、D两试管中,再分别倒入氯化铜溶液和硫酸铜溶液,结果C试管中产生较多气泡和紫红色固体,D试管中一段时间内无明显现象。将反复打磨了的铝片放入E试管中,加入硫酸铜溶液中产生一些气泡和紫红色固体。对比CD两试管说明_______________会影响铝与铜盐溶液的反应。为了验证这一观点,向D试管中加入下列物质中的_____________,也产生与C试管同样现象。
A.NaCl溶液 B.Na2SO4溶液 C.KCl溶液 D.稀硫酸
对比DE两试管说明________________________会影响了铝与硫酸铜的反应。
(3)向盛有氢氧化钠溶液的G、H两支试管中分别滴入酚酞试液和氯化铁溶液,G中溶液变红色,H中出现_______________________,再分别滴入稀硫酸并充分振荡,G试管中看到____________________________时说明氢氧化钠与稀硫酸恰好完全反应,H试管中则看到____________________,此中和反应有明显现象,请再举一个有明显现象的中和反应实例_________________(用化学方程式表示)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法不正确的是( )
A.镁铝合金mg和足量的盐酸反应生成H20.1g,则m可能是0.8
B.常温下,将5.6g生石灰放入94.4g水中,所得溶液中溶质质量分数小于1%
C.将镁粉和铝粉的混合物7.2g与足量的氧气充分反应,得到的氧化物质量可能为13.6g
D.将铁合金置于氧气中燃烧得到0.44g二氧化碳和29g四氧化三铁,则铁合金是钢
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com