
【题目】同学甲用排水集气法收集到几瓶无色气体,
(1)如图所示放置,请你推测该气体除颜色、状态以外的其他一些物理性质:___
![]()
(2)同学乙确定这是氧气,检验方法_____
(3)同学甲做了红磷和铁丝的性质实验,写出红磷燃烧的化学方程式_____,写出铁丝燃烧的现象:_____。
(4)乙同学为了证明质量守恒定律,点燃1g光亮镁条。反应结束后,仔细收集白色粉末称量,根据质量守恒定律,理论上应该大于1g,原因_____。乙同学实际称白色粉木小于1g,分析可能的原因_____ (不考虑误差)
(5)用加热氯酸钾和二氧化锰的混合物制取氧气,若加热反应结束产生氧气0.06mol则分解的氯酸钾的质量是多少克?(列式计算)______
【答案】密度比空气大 用带火星的木条插入集气瓶内,木条复燃 4P+5O2![]() 2P2O5 铁丝剧烈燃烧,火星四射,放出大量的热,生成黑色固体 镁条燃烧是与空气中的氧气反应生成的氧化镁 生成的白烟跑掉了一部分 4.9g
2P2O5 铁丝剧烈燃烧,火星四射,放出大量的热,生成黑色固体 镁条燃烧是与空气中的氧气反应生成的氧化镁 生成的白烟跑掉了一部分 4.9g
【解析】
(1)如图所示放置,由于瓶口向上,所以对应的物理性质:密度比空气大;
(2)同学乙确定这是氧气,由于氧气支持燃烧,所以检验方法用带火星的木条插入集气瓶内,木条复燃;
(3)同学甲做了红磷和铁丝的性质实验,红磷燃烧是红磷和氧气在点燃的条件下生成五氧化二磷,对应的化学方程式 4P+5O2![]() 2P2O5,铁丝燃烧的现象:铁丝剧烈燃烧,火星四射,放出大量的热,生成黑色固体;
2P2O5,铁丝燃烧的现象:铁丝剧烈燃烧,火星四射,放出大量的热,生成黑色固体;
(4)乙同学为了证明质量守恒定律,点燃1g光亮镁条。反应结束后,仔细收集白色粉末称量,根据质量守恒定律,理论上应该大于1g,原因镁条燃烧是与空气中的氧气反应生成的氧化镁。乙同学实际称白色粉木小于1g,分析可能的原因 生成的白烟跑掉了一部分 (不考虑误差);
(5)设分解的氯酸钾的质量为x。
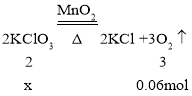
![]() x=0.04mol;
x=0.04mol;
分解的氯酸钾的质量=122.5g/mol×0.04mol=4.9g。


 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案科目:初中化学 来源: 题型:
【题目】现有25 g石灰石样品,请按下面要求计算:
(1)25 g样品与足量的稀盐酸反应放出8.8 gCO2(杂质不溶于酸,且不与酸反应),请计算该样品的纯度(CaCO3的质量分数)是多少________?
(2)若将一定质量的该石灰石样品高温煅烧,有关物质质量随反应时间的变化如表所示:
时间/min | t1 | t2 | t3 | t4 | t5 |
CO2质量/g | 2.2 | 4.4 | 6.6 | 8.8 | 8.8 |
剩余固体质量/g | 22.8 | 20.6 | m | 16.2 | 16.2 |
则m=_____,t3时剩余固体中除杂质外含有的物质是____(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某学习小组围绕“气体的实验室制取”进行研讨,请你参与完成下面的问题.

(1)图①装置制取气体的适用条件是________.
(2)图③装置相比图②装置的主要优点是________.
(3)实验室用固体和液体反应来制取O2 , 选用的发生装置________,发生反应的化学方程式是________.
(4)实验室若用图④装置收集CO2时,气体应从________端通入.(填字母)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧气是重要的资源,回答下列问题。
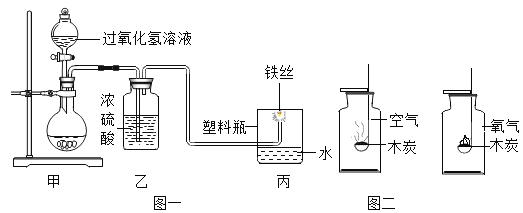
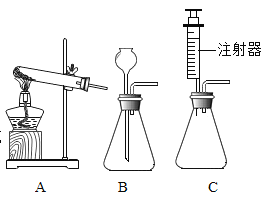
(1)图一为“铁丝在氧气中燃烧”的实验改进装置(浓硫酸具有吸水性,可干燥氧气)。图一甲装置:固体是二氧化锰,其作用是______________;发生反应的文字表达式为________;图一丙装置:铁丝在氧气中燃烧,观察到的实验现象_______________;用塑料瓶代替集气瓶的优点之一是_______。
(2)某兴趣小组为了研究用向上排空气法和排水法收集的氧气浓度是否有差异,做了如下实验:加热高锰酸钾固体,分别用两种方法各收集三瓶氧气,井使用传感器测定收集到的氧气浓度,数据见表。
收集方法 | 向上排空气法 | 排水集气法 | ||||
氧气浓度% | 79.6 | 79.7 | 79.9 | 90.0 | 89.8 | 89.3 |
氧气平均浓度% | 79.7 | 89.7 | ||||
①用向上排空气法收集氧气时,以能使放置在集气瓶瓶口的带火星木条复燃为氧气集满的标准;用排水集气法收集氧气时,以观察到____________为氧气集满的标准。
②以上两种方法中,用_________________法收集到的氧气更纯净。
③不考虑操作因素,排水集气法获得的氧气体积分数不能达到100%主要原因_____________。
④向上排空气法收集到的氧气浓度只有80%左右的原因有_________(填字母序号)。
A 氧气的密度略大于空气的密度
B 加热高锰酸钾固体产生氧气的浓度只有80%左右
C 当观察到带火星木条复燃时,集气瓶内还有空气
D.当氧气进入集气瓶时,瓶内空气与进入的氧气相互扩散
(3)分别把点燃的木炭放入装有空气和氧气的集气瓶中燃烧,如图二,对比木炭在空气和氧气中燃烧的现象,说明影响燃烧剧烈程度的一种因素是________________。
(4)在潜水艇中提供氧气的反应原理之一是:过氧化钠(固体)和水反应生成氢氧化钠和氧气,实验室中可用(如图三所示)_____ 装置来模拟其制取过程(填字母序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某班同学用如图所示装置测定空气里氧气的含量。先用弹簧夹夹住乳胶管。点燃红磷,伸入瓶中并塞上瓶塞。待红磷熄灭并冷却后,打开弹簧夹,观察广口瓶内水面变化情况。实验完毕,甲同学的广口瓶内水面上升明显小于瓶内空气体积的1/5,乙同学的广口瓶内水面上升明显大于瓶内空气体积的1/5。下列对这两种现象解释合理的是( )
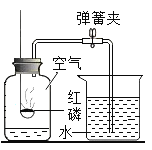
①甲同学可能使用红磷的量不足,瓶内氧气没有消耗完
②甲同学可能未塞紧瓶塞,红磷熄灭冷却时外界空气进入瓶内
③乙同学可能没夹紧弹簧夹,红磷燃烧时瓶内部分空气受热从导管逸出
④乙同学可能插入燃烧匙太慢,塞紧瓶塞之前,瓶内部分空气受热逸出
A.①③B.②④C.①②③④D.①②
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学使世界更美好,通过学习,我们有很多的收获。
收获一:世界万物都是由元素组成的,请用适当的化学符号填空:
①正三价的铝元素__________;
②硝酸钾中的原子团__________;
③人体中含量最多的物质:__________;
④植物光合作用的原料___________;
⑤海水中除了水之外,含量最丰富的物质是________。
收获二:我们学会了从宏观和微观的角度认识物质世界。
①在水、铜和氮气三种物质中,__________(填化学式)是由原子直接构成的;
②“O”和“●”表示不同元素的原子,以下图示表示单质的是__________(选填编号);
A 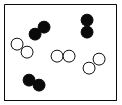 B
B 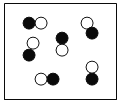 C
C 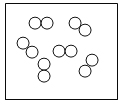 D
D 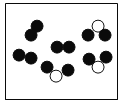
③食品中常加入防腐剂——苯甲酸钠![]() 。该防腐剂由_________;种元素组成,摩尔质量为__________;0.1mol的苯甲酸钠中约含有__________个氧原子。
。该防腐剂由_________;种元素组成,摩尔质量为__________;0.1mol的苯甲酸钠中约含有__________个氧原子。
收获三:生活中处处有化学,“家”就是一个化学小世界,蕴含丰富的化学知识。
①某矿泉水的主要矿物质成分及含量如下表:
成分 | Ca | K | Zn | F |
含量(mg/L) | 20 | 3 | 0.06 | 0.02 |
这里Ca、K、Zn、F是指_________(选填“元素、原子、单质”)。
②下表为几种家用清洁剂的功能及有效成分:
名称 | 功能 | 有效成分 |
漂白精 | 快速漂除衣物污渍 | HC1 H2O |
洁厕灵 | 有效清除污垢与异味 | HC1 NaClO |
活氧彩漂 | 漂洗使衣物色彩鲜艳 | NaClO H 2O 2 |
I.这些清洁剂属于_________(选填“混合物”或“纯净物”),若不小心把“洁厕灵”打翻在大理石地面上,会出现__________的现象;
Ⅱ.![]() 中氢、氧元素质量比为________;
中氢、氧元素质量比为________;
Ⅲ.“洁厕灵”与“漂白精”不能混用,二者混合易产生一种有毒气体X。反应原理为: ![]() ,则X的化学式为________。
,则X的化学式为________。
③玻璃中的主要成分![]() 属于__________(选填“金属氧化物”或“非金属氧化物”)。
属于__________(选填“金属氧化物”或“非金属氧化物”)。
④塑料诞生一百年来风光无限,它的发明者贝克兰也因此荣获“塑料之父”的美誉,而今由于人们使用不当而直接引发的一大环境问题是________(选填编号)。
A 沙尘暴 B 水土流失 C 温室效应 D 白色污染
⑤天然气的主要成分是甲烷![]() ,一个甲烷分子的质量约为_______克(只列式,不用计算结果)。
,一个甲烷分子的质量约为_______克(只列式,不用计算结果)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现在下列实验装置,如图1所示。回答问题:
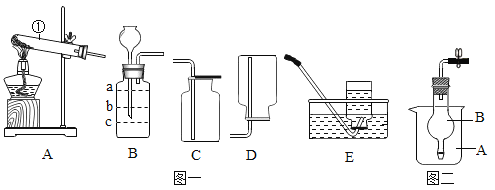
(1)仪器①的名称是____________,用于加热的仪器是_____________________。
(2)若用B装置制气体,加入液体的位置在_________处(填装置中的字母)。
(3)实验室用铁锈替代二氧化锰5%的双氧水溶液反应,发现也能快速产生气体,且反应结束后过滤出的铁锈可重复使用。请写出该反应的化学方程式________________________,铁锈在该反应中的作用是____________。
(4)现需制取0.05mol氧气,需要过氧化氢的物质的量为__________(要求写出计算过程)。若用溶质质量分数为5%的过氧化氢溶液制取上述氧气,需要溶液的质量为_________g.
(5)若实验室用氯酸钾和二氧化锰的混合物制取并收集氧气,可选择的发生装置为_________(填字母),反应的化学方程式为________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸铜溶液能对过氧化氢的分解起催化作用.某小组拟在相同浓度硫酸铜溶液的催化下,探究硫酸铜对不同浓度过氧化氢溶液分解速率的影响.
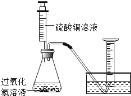
(1)分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的硫酸铜溶液,如图观察到产生气泡的速率不同,就可以粗略判断,得出实验结果.写出有关反应的化学方程式_____ ;
(2)为进一步判断上述实验结论的准确性,运用图,小刚同学进行了如下实验方案设计.
[方案一]在不同过氧化氢浓度下,测定收集相同气体体积所需时间.
[方案二]在不同过氧化氢浓度下,测定 ____________.
方案二的实验测量结果:
实验序号 物理量 | 过氧化氢溶液的浓度和体积 | 6%硫酸铜溶液的 体积(mL) | 反应的时间 (min) | 生成氧气的 体积(mL) |
1 | 8%10mL | x | 5 | V1 |
2 | 16%10mL | 3 | 5 | V2 |
表中x= _____.
实验结论:通过测量,若V1<V2,说明其它条件相同时, _________.
[继续探究]除了上述探究的影响反应速率的因素外,还有哪些因素可能会影响过氧化氢分解的反应速率?_______________(答一条即可)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铝元素与人类关系密切.
(1)铝是地壳中含量最高的_____元素.
(2)元素周 期 表中 铝 元素 的 信 息如图所示,其原子的核外电子数为_____.
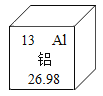
(3)铝元素在自然界中主要以Al2O3存在,Al2O3属于_____(填字母序号).
A 单质 B 氧化物 C 碱 D 盐
(4)工业用电解熔融Al2O3的方法冶炼铝,化学方程式为2Al2O3 4Al+3O2↑,该反应属于基本反应类型中的_____反应.
4Al+3O2↑,该反应属于基本反应类型中的_____反应.
(5)铝可制成蒸锅,主要利用铝的延展性和_____性.
(6)药品“氢氧化铝[Al(OH)3]”片剂能与胃酸(主要成分为盐酸)发生中和反应,治疗胃酸过多症,该反应的化学方程式为_____.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com