
【题目】如图为A、B、C三种物质的溶解度曲线,据图回答:
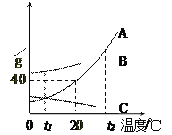
(1)将t2℃时三种物质等质量的饱和溶液分别降温到0℃时,析出溶质最多的是________。
(2)20℃时,将30 g A物质放入50 g水中,充分搅拌,所得溶液的质量是_______g。
(3)若将t1℃三种物质的饱和溶液分别升温到t2℃时,则三种溶液中溶质的质量分数由大到小的顺序是________________。
科目:初中化学 来源: 题型:
【题目】为了帮助同学们更好的理解空气中氧气含量测定的实验原理,老师利用传感器技术实时测定了实验装置(如图1)内的压强、温度和氧气浓度,三条曲线变化趋势如图2所示。下列关于此实验叙述不正确的是
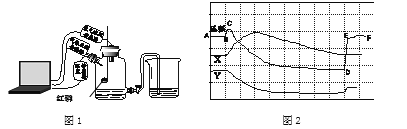
A. X曲线表示的是温度变化 B. Y曲线表示的是氧气的浓度变化
C. 图2中BC段对应的变化进程是红磷燃烧 D. 图2中CD段对应的变化进程是水倒吸进广口瓶
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向装有过量锌粉的烧杯中加入一定质量AgNO3和Cu(NO3)2的混合溶液,烧杯中固体的质量随反应时间变化的情况如图所示。下列说法正确的是

A.t1时,向溶液中滴加氯化钠溶液,没有白色沉淀产生
B.t3和t5时,溶质种类不同,金属单质种类也不同
C.若向溶液中插入铝丝,铝丝表面有红色固体析出,则时间t的取值范围是:t2<t<t4
D.t2时,溶液中的金属离子有Zn2+、Cu2+,固体中的金属单质有Zn、Ag
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列装置可制取有关气体,请回答
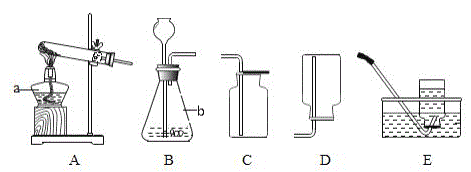
(1)仪器a、b的名称是:a_____;b_____;
(2)实验室用高锰酸钾制取氧气的化学方程式为_____,该反应的基本反应类型是_____(填“分解”或“化合”)反应;如用E装置收集氧气,当观察到_____时,再把导管口伸入盛满水的集气瓶中。
(3)实验室制取二氧化碳的化学方程式为_____,应选用的收集装置是_____
(4)如图装置可用来测量生成的O2的体积,检验该装置气密性的方法是:当把针筒里的活塞内推时,若看到_____,说明气密性良好。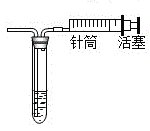
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组在制取氧气的实验过程中,有同学联想到了渔民用过氧化钙(CaO2)增加鱼池中的含氧量,于是做出猜想:过氧化钙与水反应可制取氧气。
实验装置 | 实验主要过程 |
| ①检查装置气密性。 ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体。该装置放置到第二天,集气瓶中只收集到极少量气体,震荡试管后仍有少量细小气泡缓慢放出。 |
实验结论:过氧化钙与水反应_____(填“能”或“不能”)用于实验室制取氧气。
【分析与反思】
(1)小林希望对此实验进行改进,使该反应加快,请你帮他提出合理化建议_____。
(2)同学们对过氧化钙与水反应的生成物猜想如下:①氢氧化钙和氧气②碳酸钙和氧气。你认为猜想_____(填序号)一定是错误的,理由是_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示。
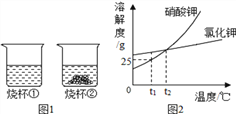
⑴ 烧杯②中的上层清液是否达到饱和状态?_______(填“是”“否”或“无法判断”)。
⑵ 烧杯①中溶解的溶质是________(写化学式)。
⑶ 将t1℃时硝酸钾的饱和溶液50g稀释成10%的溶液,需加水_________g。
⑷ 关于图1中烧杯内的物质,下列说法正确的是__________。
a.烧杯①内溶液中溶质的质量分数>烧杯②内上层清液中溶质的质量分数
b.两烧杯同时蒸发少量的水,两烧杯中都一定有固体析出
c.将两烧杯中的溶液混合到一起,充分搅拌后,烧杯中一定还有剩余固体
d.将温度升高到t2℃,两烧杯内溶液中溶质的质量分数相等(不考虑水的蒸发)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】图1是初中化学的几种常用仪器,根据要求回答问题:

(1)写出仪器C的名称________.
(2)实验室用过氧化氢溶液制取氧气,应选用的仪器是_____(填字母序号),反应的化学方程为_____________;若用稀盐酸制取二氧化碳气体,还需要的药品为________________,检验二氧化碳气体已集满的方法是_____________________________________.
(3)小明为了用图2装置收集一定量的氧气,装置接口连接的顺序为____,量筒的作用_____________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是
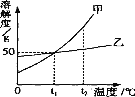
A.t1℃时,甲、乙两种物质的溶解度都是50g
B.t2℃时,在两种饱和溶液中,溶质的质量甲一定大于乙
C.t2℃时,将甲的饱和溶液降温至t1℃,其溶质的质量分数减小
D.t1℃时,将30g甲放到50g水中,所得溶液的溶质质量分数为37.5%
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】肼(N2H4)是氮和氢形成的化合物,易溶于水。工业上利用尿素法生产肼,同时得副产品十水碳酸钠,工艺流程如下:
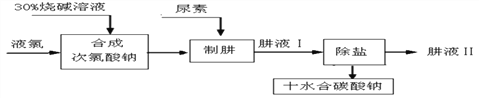
(资料)①尿素的化学式为CO(NH2)2; ②Cl2+H2O==HCl+HClO;
③制肼过程的反应为CO(NH2)2+NaClO+2NaOH==N2H4+Na2CO3+NaCl+H2O;
下列说法不正确的是
A. 尿素不能与熟石灰、草木灰等碱性物质混合使用,会生成氨气,造成肥效流失
B. Cl2与NaOH溶液发生反应的化学方程式为Cl2+2NaOH==NaCl+NaClO+H2O
C. 从母液中分离出十水合碳酸钠晶体,可采用蒸发浓缩、冷却结晶、过滤、洗涤干燥等步骤
D. 从后续反应过程来看,若要使原料利用率最佳,合成次氯酸钠时投入的液氯与烧碱的质量之比为71 :80
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com