
| 反应时间 | t0 | t1 | t2 | t3 |
| 烧杯和药品的质量/g | 166.5 | 166.3 | 166.1 | 166.1 |
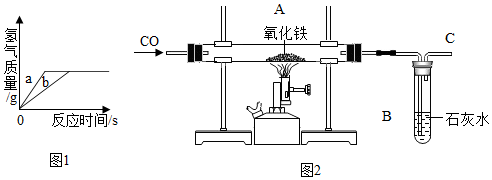
分析 (1)由已知:“用质量相等的镁粉和铝粉,分别与溶质质量分数相同、等质量的稀盐酸充分反应”,若酸完全反应,金属都剩余,则生成氢气相等,若金属完全反应,则生成氢气一定不相等.
(2)回顾一氧化碳还原氯化铁的实验,回答对该实验的操作所提出的问题.
(3)由表中的实验数据可判断第四次称量时已完全反应,利用质量守恒定律,可计算放出氢气的质量;
根据化学方程式求出铁的质量,进而求出①.
解答 解:(1)根据化学方程式:Mg+2HCl=MgCl2+H2↑;2Al+6HCl═2AlCl3+3H2↑进行计算可知:
A、因为镁的活动性比铝的活动性强,镁反应速度快,故A说法正确;
B、如果盐酸均反应完,镁恰好完全反应,铝有剩余,故B说法正确;
C、如果镁、铝都反应完,则产生的氢气一定不等,说法不正确.
D、盐酸均反应完,镁、铝都反应完,生成的氢气一定相等,故D说法正确;
故选AB
(2)一氧化碳还原氧化铁生成铁和二氧化碳,故看到的现象为固体由红变黑,澄清石灰水变浑浊,为防止生成的铁被氧化,实验结束前还要继续通一氧化碳直到冷却,故不需要断开;
(3)由质量守恒定律可知,生成氢气的质量=反应前总质量一反应后总质量=11.5+100g+55g-166.1g=0.4g
设铁的质量为x
Fe+H2SO4 =FeSO4 +H2↑;
56 2
x 0.4g
$\frac{56}{x}=\frac{2}{0.4g}$
解得:x=11.2g
原生铁样品中铁的质量分数=$\frac{11.2g}{11.5g}$×100%=97.4%
故答案为:(1)AB;
(2)①A 固体由红变黑,B 石灰水变浑浊,②不需要,气体会一直通到装置冷却,不会发生倒吸;
(3)①0.4;②原生铁样品中铁的质量分数是97.4%.
点评 本题为涉及较多的化学基础知识,题目难点不大但涉及面较广,耐心审题、沉着作答对于解答类似问题会有较大帮助.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将50.0mL酒精与50.0mL蒸馏水混合,所得溶液体积小于100.0mL | |
| B. | 铁丝在氧气中燃烧,剧烈燃烧、火星四射、放热,生成四氧化三铁 | |
| C. | “粗盐提纯”实验中,过滤时将悬浊液直接倒入漏斗 | |
| D. | 硫在空气中燃烧发出明亮蓝紫色火焰,生成无色无味气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 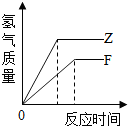 表示向足量的稀HCl中加入等质量的锌和铁,生成氢气质量和反应时间的关系图 | |
| B. | 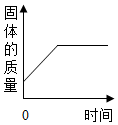 表示CO还原Fe2O3的实验中,试管内的固体质量与时间的关系图 | |
| C. | 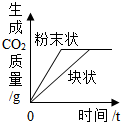 表示等质量CaCO3分别与等体积等质量分数的稀盐酸(足量)反应 | |
| D. |  表示向足量的稀HCl中加入少量Fe,溶液质量与时间的关系图 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 物质 | 甲烷 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 3.2 | 11.2 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
| A. | 表中a的值为2.8 | B. | X一定是该反应的催化剂 | ||
| C. | X可能含有氢元素 | D. | X一定含有氧元素 |
查看答案和解析>>
科目:初中化学 来源:2017届湖北省襄阳市保康县九年级中考适应性考试化学试卷(解析版) 题型:信息分析题
分析、归纳、总结是学习化学的有效方法.
(1)用“三”总结化学知识如下:
①复分解反应发生的三个条件是:生成沉淀或生成________________或生成水;
②燃烧的三个条件是有可燃物、氧气(或空气)和_______________.
③铁生锈的三种反应物质是:铁、水和___________;
(2)在C + 2CuO 2Cu + CO2↑与CO + CuO
2Cu + CO2↑与CO + CuO  Cu + CO2两个反应中,C和CO都是将CuO还原为Cu的物质,故在该反应中作还原剂.
Cu + CO2两个反应中,C和CO都是将CuO还原为Cu的物质,故在该反应中作还原剂.
①上述两个反应中还原剂的化合价变化规律:_______________.
②根据你的规律,判断反应Fe+H2SO4=FeSO4+H2↑中的还原剂是_______________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com