
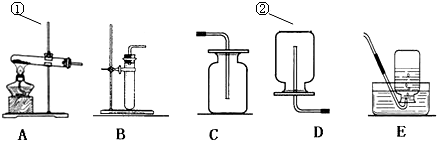
| A. | 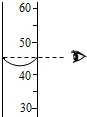 液体读数 | B. |  滴加液体 | C. | 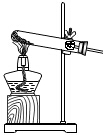 加热固体 加热固体 | D. | 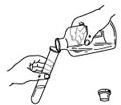 倾倒液体 |
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
| A. | 溶质质量减小 | B. | 溶液仍为t℃时的饱和溶液 | ||
| C. | 溶质在t℃时的溶解度不变 | D. | 溶液质量不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验编号 | 1 | 2 |
| 反应物 | 5% H2O2 | 5%H2O2 |
| 催化剂 | 1g水泥块 | 1g二氧化锰 |
| 时间 | 165s | 46s |
| 实验步骤 | 现 象 | 结 论 |
| 取一支试管加入3mL5%的过氧化氢溶液,然后加入少量二氧化锰. | 缓慢有少量气泡冒出 | 浓度越大,过氧化氢分解的速率越快 |
| 另取一支试管加入3mL15%的过氧化氢溶液,然后加入少量二氧化锰. | 迅速有大量气泡冒出 |
| 实验步骤 | 现 象 | 结 论 |
| 取一支试管加入5mL 15%的过氧化氢溶液.然后把试管放入盛有冷水的烧杯中; 取一支试管加入5mL 15%的过氧化氢溶液.然后把试管放入盛有热水的烧杯中 | 缓慢有少量气泡冒出; 迅速有大量气泡冒出 | 温度越高,过氧化氢分解的速率越大 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②④⑥ | C. | ③ | D. | ⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
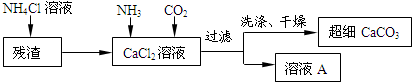
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com