

 CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O 2CuSO4+2H2O
2CuSO4+2H2O

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:初中化学 来源: 题型:

 1调整天平零点时,若指针偏向左边,应将左边的平衡螺母向
1调整天平零点时,若指针偏向左边,应将左边的平衡螺母向查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
. |
查看答案和解析>>
科目:初中化学 来源:专项题 题型:实验题

 CuSO4+SO2↑+2H2O.从环保和经济的角度分析,对比途径I、Ⅱ,途径I的优点有:不产生有害气体和 _________ .
CuSO4+SO2↑+2H2O.从环保和经济的角度分析,对比途径I、Ⅱ,途径I的优点有:不产生有害气体和 _________ .
查看答案和解析>>
科目:初中化学 来源:2012年江苏省苏州市高新区中考化学一模试卷(解析版) 题型:解答题

 CuSO4+SO2↑+2H2O.从环保和经济的角度对比分析途径I、II,途径I的优点有:不产生有害气体和______.
CuSO4+SO2↑+2H2O.从环保和经济的角度对比分析途径I、II,途径I的优点有:不产生有害气体和______.查看答案和解析>>
科目:初中化学 来源:2011年江苏省南京市溧水县中考化学二模试卷(解析版) 题型:解答题

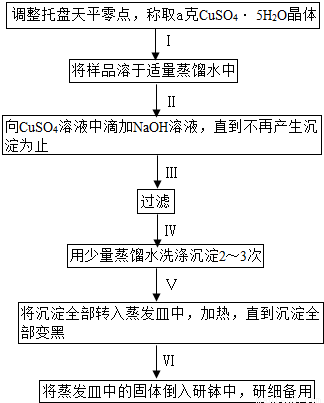
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com