
| A. | 碱溶液呈碱性,所以呈碱性的溶液一定是碱溶液 | |
| B. | 氧化钙和水反应生成氢氧化钙,所以氧化铁和水反应生成氢氧化铁 | |
| C. | 金属铝与盐酸反应生成AlCl3和H2,所以金属铁与盐酸反应生成FeCl3和H2 | |
| D. | 二氧化碳和烧碱反应生成碳酸钠和水,所以三氧化硫和烧碱反应生成硫酸钠和水 |
分析 A、根据显碱性的溶液可能是碱溶液、盐溶液等,进行分析判断.
B、根据氧化钙能水反应,氧化铁难溶于水,不与水反应,进行分析判断.
C、根据金属的化学性质,进行分析判断.
D、根据碱能与一些非金属氧化物反应,进行分析判断.
解答 解:A、碱溶液一定呈碱性,呈碱性的溶液不一定是碱溶液,也可能是碳酸钠等盐溶液,故选项推断错误.
B、氧化钙和水反应生成氢氧化钙,但氧化铁难溶于水,不与水反应,故选项推理错误.
C、金属铝与盐酸反应生成AlCl3和H2,所以金属铁与盐酸反应生成FeCl2和H2,故选项推理错误.
D、二氧化碳和烧碱反应生成碳酸钠和水,三氧化硫和烧碱反应生成硫酸钠和水,故选项推理正确.
故选:D.
点评 本题难度不大,掌握显碱性的物质可能是碱溶液或盐溶液、金属与碱的化学性质等是正确解答本题的关键.


科目:初中化学 来源: 题型:选择题
 | 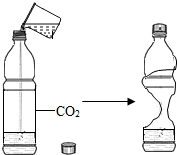 |  |  |
| A.同一物质在不同溶剂 中的溶解性不同 | B.二氧化碳与水 反应生成碳酸 | C.白磷着火点 比红磷低 | D.分子在不断运动 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 序号 | 实验步骤 | 实验现象 | 实验结论 |
| ① | 取部分固体于试管中,加人足量的水,在试管口播人带火星的木条; | 固体完全溶解, 木条复然 | 假设3不成立 |
| ② | 取少量①中溶液于试管中,滴加足量的稀盐酸,振荡. | 有气泡生成 | 假设2成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 选择的试剂 | 预期现象 | 反应的化学方程式 |
| Ca(OH)2溶液 | 一支试管无明显现象; 另一支试管产生白色沉淀(出现白色浑浊) | Ca(OH)2+Na2CO3=CaCO3↓+2NaOH |
| 实验现象 | 结论 |
| 溶液沾在试纸上时,试纸缓慢地变色 | 与标准比色卡对比,Na2CO3溶液pH=3 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 洗发精(pH=8) | B. | 厕所清洁剂(pH=1) | C. | 洗衣液(pH=10) | D. | 厨房清洁剂(pH=13) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 15g | B. | 10g | C. | 20g | D. | 25g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com