
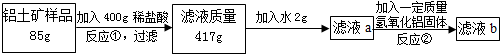
分析 (1)根据氧化铝和盐酸反应生成氯化铝和水进行分析;
(2)(3)根据参加反应的盐酸质量和铝土矿的质量,可以求出参加反应的氧化铝的质量,然后再求出氯化铝的质量;
(4)根据铝土矿消耗的盐酸,求出剩余的盐酸,然后再结合化学方程式计算出加入的氢氧化铝的质量;
(5)根据化学方程式求出两次反应生成的氯化铝,在求出溶液的质量,然后依据质量分数的计算公式进行解答;
(6)根据溶液稀释前后,溶质质量不变进行分析.
解答 解:(1)氧化铝和盐酸反应生成氯化铝和水,化学方程式为:Al2O3+6HCl=2AlCl3+3H2O;
(2)根据质量守恒定律可知,参加反应的氧化铝的质量为:417g-400g=17g,所以$\frac{17g}{85g}$×100%=20%;
设生成的氯化铝质量为X,需要盐酸的质量为y
Al2O3+6HCl=2AlCl3+3H2O
102 219 267
17g y X
$\frac{102}{17g}$=$\frac{267}{X}$=$\frac{219}{y}$
y=36.5g
X=44.5g
所以盐酸的质量分数为:$\frac{36.5g}{200g}$×100%=18.25%;
所以与氢氧化铝反应的盐酸的质量为:200g×18.25%=36.5g,
需要的氢氧化铝为z,生成氯化铝为m
Al(OH)3+3HCl=AlCl3+3H2O
78 109.5 133.5
z 36.5g m
$\frac{78}{z}$=$\frac{219}{36.5g}$=$\frac{267}{m}$
z=26g
m=44.5g
所以滤液b的质量分数为:$\frac{44.5g+44.5g}{417g+2g+13g}$×100%=20%;
(6)需加水的质量为:400g-$\frac{400g×18.25%}{36.5%}$=200g.
故答案为:(1)Al2O3+6HCl=2AlCl3+3H2O;
(2)$\frac{102}{17g}$=$\frac{267}{X}$;
(3)20%;
(4)26g;
(5)20%;
(6)200g.
点评 在解此类题时,首先分析题中的反应原理,然后结合题中所给的数据进行解答,注意质量守恒定律的应用.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 杂质 | 除去杂质的方法 |
| A | O2 | CO2 | 通过碱石灰 |
| B | Cu粉 | Fe粉 | 加入过量稀盐酸,过滤 |
| C | CO2 | CO | 通入氧气点燃 |
| D | FeCl2溶液 | CuCl2 | 加过量Fe粉,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| Ⅰ取少量灰白色固体于盛有足量 水的烧杯中,充分反应并用 湿润的酚酞试纸检验生成的气体, 然后过滤,滤渣用蒸馏水洗涤. | 固体部分溶于水,产生气泡 湿润的酚酞试纸变红. | 猜想1不成立 猜想2、猜想3可能成立 |
| Ⅱ取实验I中的滤渣于试管中 加入足量的稀盐酸. | 产生气泡. | 结合实验Ⅰ,猜想3成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 空气中的氧气约占空气体积的$\frac{1}{5}$ | |
| B. | 空气中的氮气常用作保护气 | |
| C. | 空气中的稀有气体常用作灭火剂 | |
| D. | 空气中的二氧化碳是植物光合作用的原料 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com