
【题目】还原铁粉是结构疏松的单质铁,是重要的工业原料。
I.物质制备。还原铁粉的某种制备工艺流程如下:
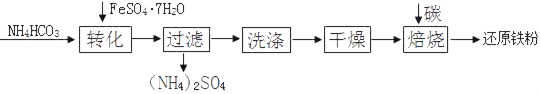
(1)“转化”时温度需控制在35℃以下,防止受热分解的物质是_____。
(2)“干燥”过程中有少量的FeCO3转化为FeOOH和CO2,此时与FeCO3反应的物质有_____(填化学式)
(3)FeCO3和 FeOOH在空气中焙烧转化为Fe2O3,FeOOH转化为Fe2O3的反应类型是_____。写出Fe2O3在高温条件下与碳(C)反应生成Fe和CO2的化学方程式:_____。
Ⅱ.成分研究。“暖宝宝”一般由还原铁粉、活性炭和氯化钠等组成。
(实验目的)测定未开启的“暖宝宝”中铁的质量分数。
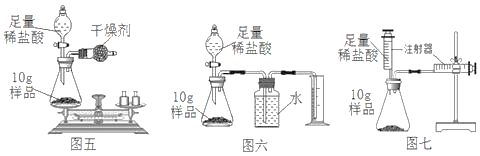
(实验过程)如图五所示,甲同学称得反应前总质量为85g,打开活塞待稀盐酸全部滴入后立即关闭活塞。锥形瓶内的现象有:固体逐渐减少,_____。反应完毕后测得锥形瓶和反应后混合物的总质量为84.8g。
(评价反思)
(1)乙同学认为甲同学方案误差较大,于是设计如图六的方案。甲同学方案误差较大的原因是_____。
(2)丙同学认为乙同学方案即使操作无失误,测量结果仍会偏大,原因是_____。
(3)丙同学设计了图七的实验装置。利用该装置实验时,在气密性良好的前提下,如果往锥形瓶中注入的稀盐酸体积为V1mL,等充分反应并且待装置冷却后,观察右侧注射器读数増加V2mL.实验条件下氢气密度为 d g/mL.则样品中铁的质量分数为_____。
【答案】碳酸氢铵 H2O、O2 分解反应 2Fe2O3+3C![]() 4Fe+3CO2↑ 。 产生大量气泡,溶液由无色变为浅绿色 反应前装置内气体为空气,反应后装置内气体是氢气,相同体积的氢气质量比空气小得多 。 分液漏斗中的稀盐酸进入锥形瓶会排出一定体积的气体 。 280(V2﹣V1)d% 。
4Fe+3CO2↑ 。 产生大量气泡,溶液由无色变为浅绿色 反应前装置内气体为空气,反应后装置内气体是氢气,相同体积的氢气质量比空气小得多 。 分液漏斗中的稀盐酸进入锥形瓶会排出一定体积的气体 。 280(V2﹣V1)d% 。
【解析】
I、(1)“转化”时温度需控制在35℃以下,碳酸氢铵受热易分解,所以防止受热分解的物质是碳酸氢铵,故填碳酸氢铵。
(2)“干燥”过程中有少量的FeCO3转化为FeOOH和CO2,根据生成物有氢元素且铁的化合价升高,则一定含有氧化剂,所以此时与FeCO3反应的物质有 H2O、O2,故填H2O、O2。
(3)FeCO3和 FeOOH在空气中焙烧转化为Fe2O3,FeOOH转化为Fe2O3时,根据质量守恒定律可得还生成水,对应的化学方程式为2FeOOH![]() Fe2O3+H2O,属于一变多,属于分解反应,故填分解反应。
Fe2O3+H2O,属于一变多,属于分解反应,故填分解反应。
Fe2O3在高温条件下与碳(C)反应生成Fe和CO2,故反应的化学方程式写为:2Fe2O3+3C![]() 4Fe+3CO2↑。
4Fe+3CO2↑。
Ⅱ、(1)铁与稀盐酸反应时的现象是产生大量气泡,溶液由无色变为浅绿色,故填产生大量气泡,溶液由无色变为浅绿色。
(2)甲同学方案误差较大的原因是反应前装置内气体为空气,反应后装置内气体是氢气,相同体积的氢气质量比空气小得多,故填反应前装置内气体为空气,反应后装置内气体是氢气,相同体积的氢气质量比空气小得多。
(3)丙同学认为乙同学方案即使操作无失误,测量结果仍会偏大,原因是分液漏斗中的稀盐酸进入锥形瓶会排出一定体积的气体,故填分液漏斗中的稀盐酸进入锥形瓶会排出一定体积的气体。
(4)解:生成氢气的体积为(V2﹣V1)mL,则生成氢气的质量为(V2﹣V1)mL×d g/mL
设样品中铁的质量分数为x
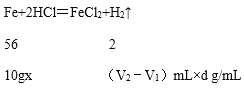
56:2=10gx:((V2﹣V1)mL×d g/mL)
x=280(V2﹣V1)d%
答:样品中铁的质量分数为280(V2﹣V1)d%。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】A~L是初中化学常见物质,它们之间的转化关系如图所示(反应条件已略去)。其中G是大理石的主要成分,A和I为红色固体,B、D和L为气体。请回答下列问题:
(1)反应①的化学方程式为_____。
(2)E的组成元素在化合物中常呈现的化合价有_____。
(3)图中涉及的反应中属于置换反应的是_____(填序号)。
(4)上述转化中,B和L表现出相似的化学性质是_____。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧气、二氧化碳是我们身边常见的物质。某兴趣小组对这两种气体研究如下:
Ⅰ.氧气、二氧化碳的制备:
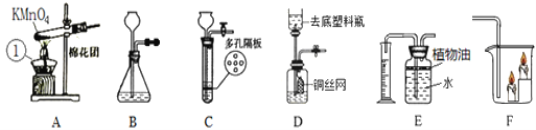
(1)写出A图中有标号仪器①的名称:__________。
(2)写出用KMnO4制取O2的化学方程式___________________,该装置中棉花团的作用是__________,图中装置一处明显的错误是__________。
(3)在化学实验室中用石灰石和稀盐酸来制取二氧化碳可选用图B所示的发生装置,该反应的化学方程式是__________。
(4)制二氧化碳也可选用如图C所示的装置,与B装置相比,C装置的优点是_________,用图D装置也可以制取二氧化碳,将石灰石放在铜丝网中,该实验说明了铜____(填“能”或“不能”)和稀盐酸发生反应。
Ⅱ.二氧化碳的性质及氧气的收集研究:
(1)二氧化碳的性质研究
①如图E所示的装置可以测定一段时间收集的二氧化碳的体积,植物油的作用是____。
②如图F所示的装置说明了二氧化碳具有__________的性质,该性质在实际生活中的应用是__________。
③已知:CO2和SO2既有相似性,又有差异性。
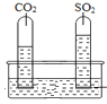
实验一:将收集满两种气体的试管同时倒立于盛水的水槽中,片刻后实验现象如图所示,说明相同条件下SO2比CO2__________(填“易”或“难”)溶于水。
实验二:已知镁条可以在CO2中剧列燃烧: 2Mg+CO2![]() 2MgO+C,试推测镁条在SO2中燃烧的现象为:剧烈燃烧,__________。
2MgO+C,试推测镁条在SO2中燃烧的现象为:剧烈燃烧,__________。
(2)氧气的收集
(实验1)用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃时停止收集,测定瓶中氧气的含量,重复实验3次。
(实验2)用向上排空气法收集氧气,当放置在集气瓶口带火星木条复燃后,继续收集40秒,测定瓶中氧气的含量,重复实验3次。
(实验3)用排水法收集氧气,测定瓶中氧气的含量,重复实验3次。
实验数据:
实验1 | 实验2 | 实验3 | |||||||
氧气的体积分数(%) | 79.7 | 79.6 | 79.9 | 88.4 | 89.0 | 87.9 | 90.0 | 89.8 | 89.3 |
氧气的平均体积分数(%) | 79.7 | 88.4 | 89.7 | ||||||
数据①由实验1、2可知,用向上排空气法收集氧气时,为提高获得的氧气体积分数,可采取的措施是__________。
②不考虑操作因素,实验3获得的氧气体积分数不能达到100%的主要原因是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】二氧化碳能与过氧化钠(Na2O2,淡黄色固体)在常温下反应产生氧气,并生成碳酸钠,且伴有能量的释放。
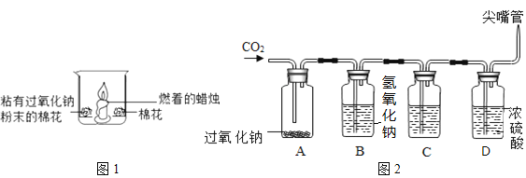
(1)如图1所示,在空气中放置时,两团棉花均不燃烧;若将足量二氧化碳倒入烧杯时,可以观察到的现象有:①______;②粘有过氧化钠的棉花燃烧;③未粘有过氧化钠的棉花不燃烧。通过上述实验的对比分析,写出产生现象②的原因______。
(2)为验证二氧化碳能与过氧化钠在常温下反应产生氧气,设计了图2实验(氢氧化钠溶液能与二氧化碳反应;浓硫酸有吸水性,且既不与二氧化碳反应,也不与氧气反应)。
①B瓶的作用是吸收未反应完的二氧化碳,C瓶的作用是检验二氧化碳是否被B瓶吸收完,则C瓶中盛放的溶液是______(写名称)。
②为验证过氧化钠和二氧化碳反应生成氧气,采用的验证方法是______。
③写出过氧化钠和二氧化碳反应的化学方程式_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】石墨烯是一种由碳原子构成的新型材料。
(1)石墨烯可作为纳米集成电路的散热材料、新型电池电极材料,这分别利用了石墨烯的性质是:_____、_____(填序号)。
A.机械特性 B.导热性 C.导电性
(2)石墨烯和纳米碳管可形成疏松多孔的“碳海绵”,类似于活性炭,具有_____性,在污水处理领域大有作为。
(3)石墨烯可看作将石墨的层状结构一层一层地剥开得到的单层碳原子。石墨烯和石墨具有相似的化学性质的原因是_____。
(4)将甲烷(CH4)在镍或铜等金属基体上高温分解,碳原子会沉积在金属表面连续生长成石墨烯,该反应的化学方程式为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图中装置适当组合可用于氧气、氢气、二氧化碳等气体的制备和收集。
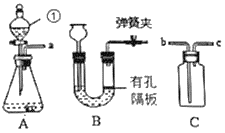
(1)仪器①的名称是_____。
(2)若用A装置制取氧气,反应的化学方程式为:_____,该反应属于_____(填基本类型)。
(3)在制取二氧化碳的实验中,装置B与装置A相比,优点是_____。
(4)C装置正放桌面,用于收集A装置中生成的氧气,则a接_____(选填b”或“c”):若将C装满水,用于收集A装置中生成的氢气,则a接_____(选填“b”或“c”)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知:常温下,CO2难溶于饱和NaHCO3溶液。下图A-D是实验室中常见装置,回答下列问题。
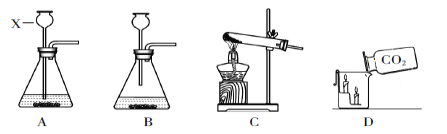
(1)仪器X的名称是__________。
(2)实验室制取CO2应选用的发生装置是_______(填字母序号),反应的化学方程式是_______。
(3)常温下,下列收集CO2的方法中可行的是____________(填字母序号)。
a.排饱和NaHCO3溶液法b.向下排空气法 C .向上排空气法 D.排水法
(4)某同学进行图D所示的操作时,观察到高的蜡烛先熄灭,其原因可能是_________。
(5)实验室用高锰酸钾制取气体时,应对C装置进行必要的改进是_________, 该反应的化学方程式为______。
(6)实验室取用药品要注意节约,如果没有说明用量,一般应该取用最少量,固体药品只需盖满试管底部,液体药品取用______mL。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氮气是一种重要的工业原料,广泛应用于化肥等工业。工业常用PSA变压吸附制氮气,某学习小组查阅到相关制氮气工艺流程,并展开学习,请回答相关问题:
(资料):
(1)、碳分子筛对不同气体的吸附强度不同,如图所示;
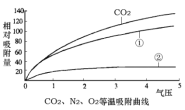
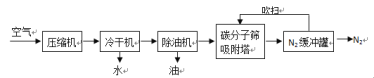
(2)、气压越大,碳分子筛吸附能力越强,反之越弱;
(3)、碳分子筛可以再生,能重复使用。
①请由高到低依次写出地壳中含量(质量分数)排在前五位的元素符号_______
②根据工艺流程,资料1图像中气体①是_______
③碳分子筛再生的方法是_______
④N2和H2在500℃、200MPa及催化剂的条件下发生反应,生成NH3,反应的化学方程式为_________,氨气中氮元素的化合价是________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】Ⅰ空气是一种用途很多的自然资源,可用于工业上制取氧气,其流程如下:
(查阅资料)常温下,氧气的沸点是-183℃,氮气的沸点是-196℃.
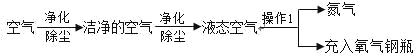
(1)操作 1 的名称是________________
(2)如果将燃着的木条置于盛满液态空气的容器口,观察到的现象是木条_____(填“熄灭”或“燃烧更旺”),一段时间后,剩余液态物质的颜色逐渐变为______________色。
(3)除分离液态空气外,现在还有一种膜分离技术制氧气,原理是在一定压力下,让空气通过薄膜,氧气能透过薄膜,从而达到分离空气的目的。据此推测氮分子比氧分子体积_________(填“大”或“小”)
(4)下列属于氧气用途的是____________(填序号)
A.气体肥料 B.工厂炼制 C.充气包装 D.霓红彩灯
Ⅱ甲、乙、丙为初中化学上册中常见物质,它们之间均能一步实现如图所示的转化关系。
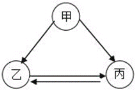
(1)如果丙能使带火星木条复燃,则甲的名称为_____,乙![]() 丙的基本反应类型是____________
丙的基本反应类型是____________
(2)如果乙是一种易与血液中的血红蛋白结合的有毒气体,则甲___________(填“肯定”或“可能”)是一种单质,若乙![]() 丙的反应现象之一是黑色变成亮红色,则化学方程式是__________
丙的反应现象之一是黑色变成亮红色,则化学方程式是__________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com