
| A. | H2SO4 | B. | HCl | C. | Cu(OH)2 | D. | Ca(OH)2 |
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| (1)分别取A、B、C、D溶液少量于试管中,两两混合 | A、B混合产生大量气泡,C、D混合无明显现象 | A、B是Na2CO3、稀盐酸溶液中的一种, C、D是Ca(OH)2、NaCl溶液中的一种 |
| (2)各取A、B、C、D溶液于四支试管中,分别滴加两滴无色酚酞试液,振荡 | A、D变红,B、C无明显现象 | A为Na2CO3溶液; C为NaCl溶液;由此区分出B、D溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H2SO4 NaCl Na2CO3 CaCl2 | B. | HCl NaOH CuSO4 MgSO4 | ||
| C. | Na2CO3 K2SO4 BaCl2 HCl | D. | NaNO3 HCl CaCl2 KOH |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

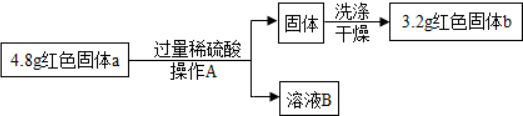
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 若三支试管中都出现白色沉淀时,则最后加入的是硝酸银溶液 | |
| B. | 若三支试管中的观象分别为产生气泡、白色沉淀、无明显变化,则最后加的是稀盐酸 | |
| C. | 若两支试管中出现气泡,一支试管中出现白色沉淀时,则最后加入的是碳酸钠溶液 | |
| D. | 若两支试管中出现白色沉淀,一支试管中无明显变化时,则最后加入的是氯化钡溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 滤渣中的物质至少有两种 | |
| B. | 取反应后的滤液滴加稀盐酸,有白色沉淀产生 | |
| C. | 取滤渣滴加稀硫酸,一定有气泡产生 | |
| D. | 取反应后的滤液观察,滤液不可能呈蓝色 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:推断题
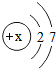 元素的性质与原子结构密切相关,请填空:
元素的性质与原子结构密切相关,请填空:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com