
【题目】在氢氧化钠溶液和稀盐酸的反应中,小明和老师用数字化设备测定了溶液温度及pH值随时间变化变化的关系曲线图。
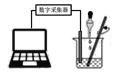
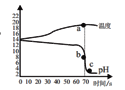
(1)根据曲线图,可知该实验是将_______(选填“氢氧化钠溶液”或“稀盐酸”)滴加到另外一种试剂中。该反应为___________。
A 吸热反应 B 放热反应
(2)a为温度曲线上的最高点,a、b两点对应的时间相同,则b对应的纵坐标数值为____。
(3)分别取样,依次进行以下实验:
①将b点处溶液中的溶质结晶,采用__________方法。
②取c点样品于试管中,加足量水稀释后溶液的pH__________7(填“>”、“<”或“=”)。
(4)若发现氢氧化钠溶液试剂瓶敞口放置,经检验该试剂中含有碳酸钠,请设计实验检验该样品中仍含有氢氧化钠_______。
(5)将50g稀盐酸加入50g氢氧化钠溶液中恰好完全反应,所得溶液中溶质的质量分数为5.85%。试计算氢氧化钠溶液中溶质的质量分数_______。
【答案】稀盐酸 B 7 蒸发结晶 < 取少量的溶液于试管中,加入过量氯化钙溶液,再取上层清液,滴加几滴酚酞观察溶液颜色变化,若变红色,则证明仍有氢氧化钠 8%
【解析】
(1)根据曲线图,未滴加时pH大于7,说明一开始是呈碱性,滴加之后pH逐渐降低至小于7,可知该实验是将稀盐酸滴加到氢氧化钠溶液中。根据温度的变化曲线,可知温度逐渐上升,说明该反应为放热反应。故填:稀盐酸;B
(2)a为温度曲线上的最高点,可知此时已经完全反应,由于a、b两点对应的时间相同,则b对应的纵坐标数值为pH值等于7。故填:7
(3)①b点处溶液中的溶质为氯化钠,由于氯化钠的溶解度随温度的变化不大,故将氯化钠结晶,采用蒸发结晶的方法来获得晶体。故填:蒸发结晶
②c点样品的溶液为酸性,取少量酸性溶液于试管中,加足量水稀释后溶液的无限接近于7但不会大于或等于7。故填:<
(4)若发现氢氧化钠溶液试剂瓶敞口放置,经检验该试剂中含有碳酸钠,由于碳酸钠溶液也为碱性,故不能直接通过测定pH值来检验是否有氢氧化钠;设计实验是:取少量的溶液于试管中,加入过量氯化钙溶液,再取上层清液,滴加几滴酚酞观察溶液是否变红,若变红色,则证明仍有氢氧化钠;故填:取少量的溶液于试管中,加入过量氯化钙溶液,再取上层清液,滴加几滴酚酞观察溶液颜色变化,若变红色,则证明仍有氢氧化钠
(5)将50g稀盐酸加入50g氢氧化钠溶液中恰好完全反应,所得溶液中的溶质为氯化钠,反应生成氯化钠的质量为(50g+50g)![]() 5.85%=5.85g;设参加反应的氢氧化钠质量为x;
5.85%=5.85g;设参加反应的氢氧化钠质量为x;
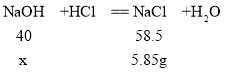
![]()
X=4g
氢氧化钠溶液中溶质的质量分数为:![]() ;
;
答:氢氧化钠溶液中溶质的质量分数为8%。故填:8%


科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种物质的溶解度曲线如图所示,根据图中信息回答下列问题
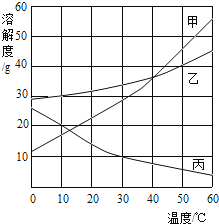
(1)50℃时,将40g乙物质放入50g水中充分溶解后,得到的溶液质量为_____g
(2)20℃时,甲、乙、丙三种物质溶解度由大到小的顺序为_____
(3)请写出一种符合丙曲线变化趋势的物质_____(填俗名)
(4)50℃时,将等质量的甲、乙、丙三种物质的饱和溶液同时降温至10℃,所得溶液中溶质质量分数最小的是_____。
(5)要配制110g溶质质量分数为9.1%的丙物质溶液,配制时溶液的温度需要控制的范围是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中国古代在认识和应用物质方面有辉煌的历史,请用恰当的化学用语填空。
(1)《本草纲目》中“灶中所烧薪柴之灰,令人以灰淋汁,取碱涴衣”中的碱为草木灰_____;
(2)《本草钢目》中“水银乃至阴之毒物,因火煅丹砂而出”水银的化学式_____;
(3)《报朴子)中记载“曾青涂铁,铁赤如铜”其曾青指硫酸铜溶液,其阳离子为_____;
(4)《天工开物》中“凡石灰,经火焚炼为用”的石灰主要成分为碳酸钙_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙的溶解度曲线。
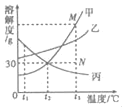
(1)t1℃时,等质量的甲、丙饱和溶液中所含溶质的质量_____(选填:甲>丙;甲<丙;甲=丙)
(2)分别将三种物质的饱和溶液从t3℃降温至t2℃时,所得溶液溶质质量分数的大小关系为_____。
(3)若要将组成在N点的甲溶液转变为M点的甲溶液,可采取方法_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】逻辑推理是一种重要的化学思维方法,下列推理中,合理的是( )
A. 因为![]() 和
和![]() 的组成元素相同,所以它们的化学性质相同
的组成元素相同,所以它们的化学性质相同
B. 因为燃烧需要同时满足三个条件,所以灭火也要同时破坏这三个条件
C. 催化剂可以加快化学反应速率,所以任何化学反应都需要催化剂
D. 有新物质生成的变化属于化学变化,所以化学变化一定有新物质生成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现欲探究一固体物质A的成分,已知其中可能含有FeCl3、CuCl2、NaCl、Ba(NO3)2中的一种或多种。按如图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全反应)。
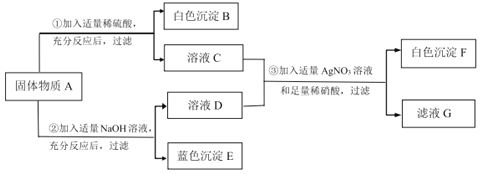
试根据实验过程和发生的现象做出判断,填写以下空白:
(1)白色沉淀B的化学式为______,白色沉淀F的化学式为______。
(2)溶液C中肯定存在的酸根阴离子是______(写离子符号)。
(3)滤液G中共存在______种溶质。
(4)一定不存在的物质是______理由是______。
(5)固体物质A中一定存在的物质是______(写化学式)。
(6)写出过程②中生成蓝色沉淀反应的化学方程式______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过碳酸钠(2Na2CO33H2O2,相对分子质量为314)是一种很好的消毒剂和供氧剂,常用于洗涤、印染、纺织、造纸、医药卫生等领域。
Ⅰ.制备过碳酸钠(查阅资料)过碳酸钠难溶于异丙醇,可浴于水,易发生反应2Na2CO33H2O2 =2Na2CO3+3H2O2;过氧化氢在温度较高时易发生分解。碳酸钠能与盐酸反应放出二氧化碳,也能与氯化钙溶液反应生成白色沉淀。
(制备流程)(图1)
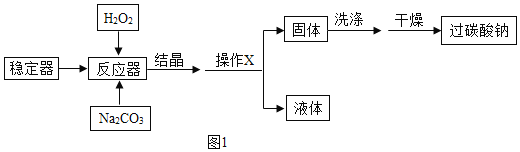
(1)操作X是________;请写出Na2CO3与H2O2化合生成过碳酸钠的化学方程式___________________________;
(2)流程中结晶在常温下进行,原因是_______________________________;
(3)为提高产品的纯度,碳酸钠和过氧化氢的最佳投料质量比是________,洗涤固体时,选用的最佳试剂是_______________ 。
(4)II.神奇的“氧立得”
小明同学新买了一台氧立得便携式制氧器,其中有A、B两包固体,经查阅资料知A包主要成分为过碳酸钠,B包为黑色固体粉未,将A包、B包药品分别放入机器,就可以制得氧气,在反应前后B的质量和化学性质不变,为探究A包固体的纯度,设计了如图2所示实验装置。
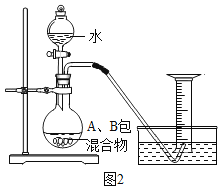
(实验步骤)①检查装置气密性;②称取2.2gA包药品和少许B包药品,并全部装入烧瓶内;③按图搭好装置;④现将橡胶管插入量筒底部;⑤打开分液漏斗;⑥待反应停止后,保持橡胶管口在量筒底部;⑦等试管冷却到室温时将橡胶管移出水槽,读取量筒读数为220mL;⑧数据处理。[氧气在实验条件下密度为1.43g/L]
(问题讨论)B固体成分为________(填化学式),实验时烧瓶内可观察到的现象是________
(5)如果将步骤④和⑤对调,实验结果将________(选填“偏大”、“偏小”或“不变”),理由是____________________________;
(6)证明反应停止后烧瓶中有碳酸钠的方法是取样加入_______,有白色沉淀产生,反应的化学方程式___________________________;
(7)此样品中过碳酸钠的质量分数为_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验台上有下列仪器(如图1):
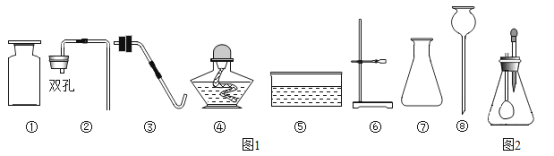
(1)制取二氧化碳,除了用到①②⑧号仪器外,还需选择的仪器是_____(填仪器名称),反应的化学方程式为_____。
(2)如图2所示,请填写适宜物质。当胶头滴管中的液体滴入到锥形瓶中时会引起气球的膨胀。
/ | A | B |
锥形瓶 | CO2 | NH3 |
胶头滴管 | _____ | _____ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com