
| A. | 用紫色石蕊鉴别硫酸溶液和硫酸钠溶液 | |
| B. | 用锌粒和稀硫酸反应制取氢气 | |
| C. | 用浓硫酸的吸水性干燥二氧化碳气体 | |
| D. | 用稀硫酸来除去铁锈 |
 寒假学与练系列答案
寒假学与练系列答案科目:初中化学 来源: 题型:填空题
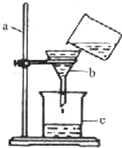 有一种含有碎菜叶、碎塑料薄膜、泥沙,还具有一定臭味的生活污水(生活污水的成分很复杂,此处已作简化),将其经除渣去臭处理后可转化为厕所的清洗用水.
有一种含有碎菜叶、碎塑料薄膜、泥沙,还具有一定臭味的生活污水(生活污水的成分很复杂,此处已作简化),将其经除渣去臭处理后可转化为厕所的清洗用水.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 在2014年南宁市理化实验操作考试中.小刚同学选择了稀盐酸、氢氧化钠溶液、酚酞溶液三种试剂,按如图所示进行酸碱中和反应的实验.请回答:
在2014年南宁市理化实验操作考试中.小刚同学选择了稀盐酸、氢氧化钠溶液、酚酞溶液三种试剂,按如图所示进行酸碱中和反应的实验.请回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 16 g | B. | 20 g | C. | 40 g | D. | 56 g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 不饱和溶液转化为饱和溶液,溶液中溶质的质量分数一定增大 | |
| B. | 将一定质量某物质的饱和溶液降温析出晶体后,所得溶液中溶质的质量一定减小 | |
| C. | 饱和溶液的浓度一定比不饱和溶液的浓度大 | |
| D. | 将5g某物质完全溶解于95g水中,所得溶液中溶质的质量分数一定是5% |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 原子在化学变化中能够再分 | |
| B. | 原子质量主要集中在原子核上 | |
| C. | 原子的质量等于核电荷数 | |
| D. | 原子的体积及在化学变化中的表现由电子决定 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作步骤 | 实验现象 | 结论及解释 |
| 步骤一:取少量固体样品于试管中,加蒸馏水完全溶解,然后加入足量的稀盐酸. | 若实验过程中始终没有气泡产生. | 则证明猜想Ⅰ成立. |
| 步骤二:取少量固体样品于试管中,加蒸馏水完全溶解,然后滴加氢氧化钡溶液. | 若实验过程中产生白色沉淀. | 则证明猜想Ⅱ或Ⅲ成立,此过程中发生反应的化学方程式为Ba(OH)2+Na2CO3═BaCO3↓+2NaOH. |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com