
 如图为常用的铁锅,回答下列问题:
如图为常用的铁锅,回答下列问题:分析 塑料属于有机合成材料;
金属具有良好的导电性、导热性和延展性;
通常情况下,铝能和空气中的氧气反应生成氧化铝;
锌比铁活泼,铁比铜活泼,铜比银活泼.
解答 解:(1)铁锅手柄上的塑料属于有机材料.
故填:有机.
(2)生活中用铁做成铁锅,是利用铁的导热性.
故填:导热.
(3)铝制品的抗腐蚀能力较铁制品强,原因是铝和空气中的氧气反应生成了氧化铝,对铝制品起到保护作用,铝和氧气反应的化学方程式为:4Al+3O2═2Al2O3.
故填:4Al+3O2═2Al2O3.
(4)将一定量铁加入到AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中,铁不能和硝酸锌反应,能和硝酸银反应生成硝酸亚铁和银,能和硝酸铜反应生成硝酸亚铁和铜,充分反应过滤,向滤渣中加入稀盐酸没有明显现象,说明滤渣中不含有铁,则滤渣中一定有铁和硝酸银反应生成的银,可能含有铜,也可能不含有铜.
故填:Ag.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.


科目:初中化学 来源: 题型:解答题
 HCl、X、CuCl2三种物质存在一定关系如图所示:(“→”表示物质间的转化关系,“-”表示两端的物质能发生化学反应).
HCl、X、CuCl2三种物质存在一定关系如图所示:(“→”表示物质间的转化关系,“-”表示两端的物质能发生化学反应).查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 A、B、C、D分别为氧化铁、盐酸、氢氧化钙、碳酸钙中的一种,它们之间的反应或转化关系如图(部分物质和反应条件已略去).则A的化学式为Ca(OH)2;反应①所属的基本反应类型为复分解反应;反应②化学方程式为Fe2O3+6HCl=2FeCl3+3H2O.
A、B、C、D分别为氧化铁、盐酸、氢氧化钙、碳酸钙中的一种,它们之间的反应或转化关系如图(部分物质和反应条件已略去).则A的化学式为Ca(OH)2;反应①所属的基本反应类型为复分解反应;反应②化学方程式为Fe2O3+6HCl=2FeCl3+3H2O.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
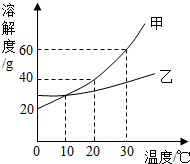 如图表示的甲、乙两种固体物质的溶解度曲线,回答:
如图表示的甲、乙两种固体物质的溶解度曲线,回答:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用燃着的木条区分二氧化碳和氨气 | |
| B. | 用燃烧的方法区别棉纤维和羊毛纤维 | |
| C. | 用肥皂水区分硬水和软水 | |
| D. | 用紫色石蕊试液区分稀盐酸和氢氧化钠溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 某化学兴趣小组进行铁生锈的实验探究活动.
某化学兴趣小组进行铁生锈的实验探究活动.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 试剂 | 白醋 | 稀盐酸 | 食盐水 | 肥皂水 | 石灰水 |
| 加入红花汁后的颜色 | 橙色 | 橙色 | 粉红色 | 绿色 | 绿色 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com