
【题目】阅读短文,回答问题。
灯的变迁
灯泡的发明给人类带来了光明,随着社会发展,我们使用的灯也在发生着变化。

1.白炽灯,白炽灯里的钨丝也害怕空气。如果玻壳里充满空气,那么通电以后,钨丝温度升高到2000°C以上,空气就会对它毫不留情地发动袭击,使它很快被烧断,同时生成一种黄白色的三氧化钨(化学式WO3),所以钨丝灯泡要抽成真空,把空气统统清除出去。有时怕抽气机抽不干净,还要在灯泡的感柱上涂一点红磷。白炽灯用久了玻壳会变黑,原因是长时间的高温使钨丝表面的钨不断地升华扩散,然后一层又一层地沉积到玻壳的内表面上,使玻壳慢慢变黑。
2.节能灯,节能灯通电时首先经过电子镇流器给灯管灯丝加热,灯丝开端发射电子(由于在灯丝上涂了一些电子粉),电子碰撞充装在灯管内的氩原子,氩原子碰撞后取得了能量又撞击内部的汞原子,汞原子在吸收能量后产生电离,灯管内构成等离子态发光。节能灯寿命长达8000小时,光效相当普通灯泡的6倍。较白炽灯节能70 ~ 80% ,低压快启,无频闪。但节能灯也有弊端,启动慢,灯管中汞也就不可避免地成为一大污染源,1只普通节能灯的含汞量约5毫克,仅够沾满一个圆珠笔尖,但渗入地下后可能造成1800吨水受污染。
3. LED灯,LED是发光二极管,是一种能够将电能转化为可见光的固态的半导体器件,它可以直接把电转化为光。白光LED的能耗仅为白炽灯的1/10,节能灯的1/4。寿命可达10万小时以上,是节能灯的10~20倍。绿色环保,不含铅、汞等污染元素,对环境没有任何污染。LED的内在特征决定了它是最理想的光源去代替传统的光源,它有着广泛的用途。
回答下列问题
(1)白炽灯变黑发生的变化是_____( 填“物理变化”或“化学变化”)。感柱上涂红磷发生反应的化学方程式是_____。
(2)LED灯与其他灯相比优点是_____。(说两点)
(3)下列说法错误的是_____。
A 节能灯内填充的只是氩气
B 这几种灯泡都能将电能转换成光能
C 白炽灯钨丝熔点大于2000℃
D LED灯在现阶段是最理想的光源
【答案】物理变化  节能,寿命长(合理即可) A
节能,寿命长(合理即可) A
【解析】
(1)白炽灯用久了玻璃壳会变黑,原因是长时间的高温使钨丝表面的钨不断地升华扩散,然后一层又一层地沉积到玻壳的内表面上,使玻壳慢慢变黑,此过程中并没有新物质生成,属于物理变化;磷与氧气在点燃的条件下反应生成五氧化二磷;化学方程式为; ;
;
(2)由题干信息可知,LED灯与其他灯相比优点是节能、使用寿命长;
(3)A.稀有气体化学性质都很稳定,常做保护气;且稀有气体在通电时可以发出特定颜色的光,常做电光源,节能灯内填充的主要是氩气,还可以是其他稀有气体,故错误;
B.这几种灯泡都能将电能转换成光能,故正确;
C.白炽灯钨丝熔点大于2000℃,故正确;
D.LED灯在现阶段是最理想的光源,故正确。
故选A。


科目:初中化学 来源: 题型:
【题目】下表是元素周期表的一部分,试回答下列问题:
第一周期 | 1H | 2He | ||||||
第二周期 | 3Li | 4Be | 5B | 6C | ① | ② | 9F | 10Ne |
第三周期 | 11Na | 12Mg | ③ | 14Si | 15P | 16S | 17Cl | 18Ar |
(1)①所示元素是__________(填“金属元素”或“非金属元素”);
(2)②所示元素与③所示元素形成的化合物的化学式是_____;
(3)下图是某元素的原子结构示意图,该原子在化学反应中易__________电子;离子符号为____________ 。

(4)下图是某元素的原子结构示意图,该元素的原子核外电子数为____。

查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】Fe2O3是一种红棕色固体,在生活、生产中有重要用途。利用废铁屑(其中杂质不溶于水,也不与酸发生反应)制备Fe2O3的流程如下:
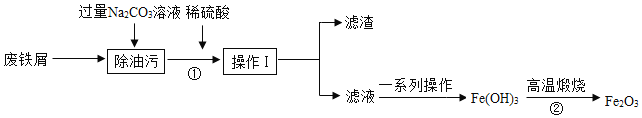
请回答下列问题:
(1)废铁屑与稀硫酸反应的化学方程式是______________。
(2)①②中未涉及的化学反应基本类型是____________。
(3)Na2CO3溶液的pH__7(填“ >”、“<”或“=”),用它除油污与用洗涤剂除油污,二者在原理上的区别是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)同学们用下图所示仪器和装置探究制取气体的方法,请回答下列问题:
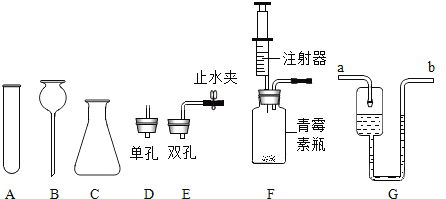
①图中仪器 B 的名称为_____。
②装配 KClO3 制备O2 的发生装置,上图中还缺少的玻璃仪器是__________(写名称),该反应的化学方程式是______________。
③图中的微型装置 F 可用于实验室制备 H2,反应化学方程式为___________。该装置在操作上的优点是_______。G 是医用输液观察滴液快慢的滴壶,若用它作微型的 O2 干燥装置,则气体应从______(填选“a”或“b”)进入,滴壶中装的试剂是_____。
(2)实验与探究是化学学习的重要方法和内容,李明看到家里多年未用的铜制火锅上有绿色的锈迹,他对绿色锈迹的成分和性质产生了浓厚兴趣。
(查阅资料)
①绿色锈迹是碱式碳酸铜[Cu2(OH)2CO3],受热易分解;
②无水硫酸铜为白色粉末,遇水变蓝;
③碱石灰是 CaO 和NaOH 的固体混合物,NaOH 与CO2反应生成碳酸钠固体和水;
④氧化铜与稀硫酸反应生成蓝色溶液,碳粉不与稀硫酸反应也不溶解在稀硫酸中。
(发现问题)
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁上有无色液滴生成.
为了进一步确定碱式碳酸铜受热分解的产物,进行了如下探究:探究一:碱式碳酸铜受热分解生成的黑色固体成分.
(猜想与假设)该黑色固体可能是①碳粉;②_____;③碳和氧化铜的混合物。
(设计方案)请帮助该同学完成下述实验报告:
实验操作与现象 | 实验结论 |
__________________________________ | 猜想②正确 |
探究二:碱式碳酸铜受热分解还会生成 CO2 和H2O.
(进行实验)选择如下图所示装置进行验证
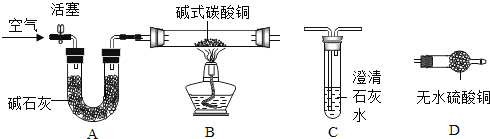
步骤一:连接A 和 B,打开活塞,通入一段时间的空气;
步骤二:点燃酒精灯,依次连接装置 A→B→_____→_____(填“C”,“D”);步骤三:点燃酒精灯,观察到明显现象后,停止加热。
(解释与结论)
①当观察到_____,说明碱式碳酸铜受热分解生成了 CO2 和H2O,写出装置 C 中反应的化学方程式_________;
②写出 Cu2(OH)2CO3 受热分解的化学方程式________。
(反思与评价)
上述装置中A 的作用是_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】I.某兴趣小组在实验室模拟水厂将塘河水净化成自来水,并最终制成蒸馏水,其流程如下图所示:
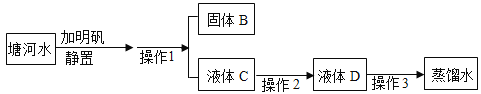
请回答下列问题:
(1)高铁酸钠(Na2FeO4)也可净水,高铁酸钠中铁元素的化合价为_____。
(2)利用如图所示的装置进行操作2,此操作的作用是_____; 待处理的水应该从_____,端通入 (填“a”或“b”),使水处理更充分。
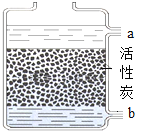
(3)取少量液体D于试管中,滴入肥皂水振荡,发现有较多的浮渣产生,说明此液体为_____ (填“软水”或“硬水”), 生活中常用_____的方法软化硬水。
(4)通过操作3可以得到净化程度较高的蒸馏水,操作3的名称是_____。
II.用水厂炉渣(主要含FeO、Fe2O3, 还有少量既不溶于水也不溶于酸的杂质)制备绿矾(FeSO4﹒7H2O)的工艺流程如下:
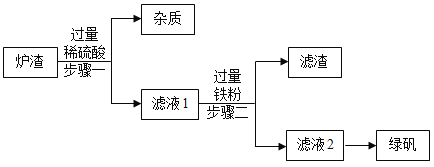
查阅资料:铁与硫酸铁反应生成硫酸亚铁。
(1)步骤一中,发生的反应之一为FeO+H2SO4= FeSO4+H2O, 其基本反应类型为_____。
(2)测得滤液2的pH明显大于滤液1,其原因是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】宏观辨识与微观探析是化学学科的重要核心素养。如图为某化学反应的微观模拟示意图,下列说法中,正确的是

A. 反应前后氧元素的化合价没有改变 B. 生成的丙、丁两物质的分子个数比为2:1
C. 该反应不属于氧化反应 D. 参加反应的甲、乙两物质的质量比为13:16
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验是进行科学探究的重要方式。

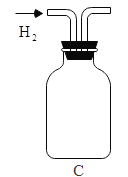
(1)写出一个用A装置来制取O2的化学反应方程式_____。
(2)若用B装置制取二氧化碳,可控制反应的发生或停止。请简述让反应停止的原理_____。
(3)若用B、C装置制取并收集氢气,请将C装置补画完整_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】水是大自然对人类的恩赐。
①水蒸发过程中,下列说法中正确的是__。(填写编号,下同)
a 水分子变大了 b 水分子间隔变大了 c 水分子在不断运动 d 水分子改变了
②水是良好的分散剂,根据图二所示甲、乙两种物质在水中的溶解度曲线,回答下列问题:
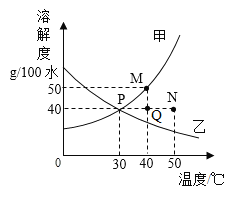
I. P点表示的含义是:___;
II.甲中混有少量乙时,提纯甲的最佳方法是__(填写编号);
a 蒸发结晶 b 恒温蒸发 c 降温结晶 d 用化学方法生成沉淀
Ⅲ.40°C时, 将30克甲放入50克水中,所得溶液的质量为__克;
IV.图中有关甲物质 M、N、P、Q 4种状态溶液的描述正确的是___。
a 都降低10°C,M、N溶质质量分数均减小
b 都恒温蒸发,M、N点均不动
c 都加入10g水,M、N点均不动
d 都升高10°C,M、N溶质质量分数均不变
e 40°C时,甲的饱和溶液中溶质质量分数为50%
f 升高10°C能使甲溶液的状态从P点转化为M点
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】丙氨酸是构成蛋白质的基本单元,如图是丙氨酸的分子结构模型,下列有关丙氨酸叙述正确的是()
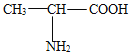
A.丙氨酸属于有机高分子化合物
B.丙氨酸分子中碳、氢元素质量比为3:7
C.丙氨酸中氧元素质量分数最大
D.一个丙氨酸分子中有13个原子核
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com