
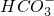 等离子.
等离子.| 物质 | Ca(HCO3)2 | Mg(HCO3)2 | Ca(OH)2 | Mg(OH)2 | CaCO3 | MgCO3 |
| 溶解性 | 可溶 | 可溶 | 微溶 | 不溶 | 不溶 | 微溶 |
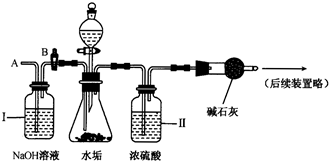


 名题金卷系列答案
名题金卷系列答案科目:初中化学 来源: 题型:阅读理解
| O | - 3 |
| 物质 | Ca(HCO3)2 | Mg(HCO3)2 | Ca(OH)2 | Mg(OH)2 | CaCO3 | MgCO3 |
| 溶解性 | 可溶 | 可溶 | 微溶 | 不溶 | 不溶 | 微溶 |

查看答案和解析>>
科目:初中化学 来源: 题型:
| 过量铁粉,过滤 |
| 适量稀硫酸,过滤 |
查看答案和解析>>
科目:初中化学 来源: 题型:
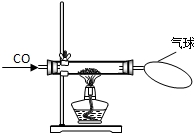 某校化学研究性学习小组的同学在学习了金属与酸的相关知识后,做了如右图所示的探究实验.实验发现CO与CuO加热后黑色粉末变成红色粉末.请你参与该小组的研究过程并完成相关任务:
某校化学研究性学习小组的同学在学习了金属与酸的相关知识后,做了如右图所示的探究实验.实验发现CO与CuO加热后黑色粉末变成红色粉末.请你参与该小组的研究过程并完成相关任务:查看答案和解析>>
科目:初中化学 来源:2008年北京市东城区中考化学二模试卷(解析版) 题型:解答题
 等离子.
等离子.| 物质 | Ca(HCO3)2 | Mg(HCO3)2 | Ca(OH)2 | Mg(OH)2 | CaCO3 | MgCO3 |
| 溶解性 | 可溶 | 可溶 | 微溶 | 不溶 | 不溶 | 微溶 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com