
科目:初中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
海洋是巨大的资源宝库,其中含有80多种元素。可以从海水中提取食盐,也可以从海水中提取用途广泛的金属镁,其制取工艺流程如下:
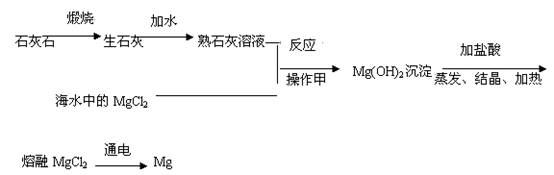
(1)从海水中提取食盐,是利用日光和风力使水分 ,得到食盐。
(2)要将Mg(OH)2沉淀分离出来,进行的操作甲的名称是 ,如果在学校实验室中完成该实验,要用到玻璃棒,其作用是 ,该操作中还需要的玻璃仪器是 和 。
(3)小明学习化学后知道,镁在氧气中燃烧会生成白色的氧化镁固体。但他在空气中点燃镁条时,却发现在生成的白色固体中还夹杂着少量的淡黄色固体。
[提出问题]为什么会生成淡黄色固体?
[查阅资料]小明查阅资料,记录了下列几种物质的颜色:
| 物 质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜 色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
其他同学认为不必查阅氯化镁的颜色,理由是 ;
[提出猜想]分析资料,小明认为淡黄色固体可能是由镁与空气中的 反应生成的;
[实验探究]小明设计实验证实了自己的猜想,他的方案可能是
;
[实验结论]根据小明的实验结果,写出镁条在空气中燃烧时两个反应的化学方程式: 、
[反思与评价]通过上述实验,你对燃烧有什么新的认识?
。
[知识拓展]由上述实验结果,若有12g镁在空气中完全燃烧,则所得产物的总质量m ___20g (填:“>”、“=”或“<”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com