
| 次数 | 1 | 2 | 3 | 4 |
| 加入氢氧化钠溶液的质量(g) | 25 | 25 | 25 | 25 |
| 生成沉淀的质量(g) | 2.9 | X | 8.7 | 8.7 |
分析 由表可以看出,加入25g氢氧化钠溶液对应的沉淀时2.9g,而第四次加入时沉淀在第三次的基础上没有增加,说明第三次已经恰好完全反应.根据沉淀的质量和对应的化学方程式求算氯化镁和生成的氯化钠的质量,进而求算对应的质量分数.
解答 解:由表可以看出,加入25g氢氧化钠溶液对应的沉淀时2.9g,而第四次加入时沉淀在第三次的基础上没有增加,说明第三次已经恰好完全反应.也可知x为5.8
设混合物中氯化镁的质量为x,生成的氯化钠的质量为y
MgCl2+2NaOH=Mg(OH)2↓+2NaCl
95 58 117
x 8.7g y
$\frac{95}{x}$=$\frac{58}{8.7g}$=$\frac{117}{y}$
x=14.25g
y=17.55g
恰好完全反应时,所得溶液的溶质质量分数为$\frac{23.7g-14.25g+17.55g}{23.7g+75g-8.7g}$×100%=30%
答:
(1)上表中X的数值是 5.8;
(2)原固体混合物样品中氯化镁的质量为14.25g;
(3)恰好完全反应时,所得溶液的溶质质量分数是30%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | 一定含有Ag+ | B. | 一定含有Ba2+ | ||
| C. | 一定含有Ag+和SO42- | D. | 可能含有Ag+或SO42-中的一种 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
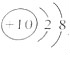 氖原子第一电子层上排布2个电子;
氖原子第一电子层上排布2个电子;查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | a点表示t2℃时100g饱和溶液中最多溶解甲物质25g | |
| B. | 将t2℃甲、乙的饱和溶液恒温蒸发溶剂,甲析出晶体多 | |
| C. | t1℃时,甲、乙两物质的饱和溶液中含溶质的质量相等 | |
| D. | 升高温度可将甲的饱和溶液变成不饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
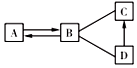 A、B、C、D为初中化学常见的四种化合物,它们之间有如图所示的转化和反应关系(“→”表示一种物质可转化为另一种物质.“-”表示相连两物质能发生化学反应).其中A、B常温下是气体且组成元素相同,C、D是同类物质,在生产生活中应用广泛.回答下列问题:
A、B、C、D为初中化学常见的四种化合物,它们之间有如图所示的转化和反应关系(“→”表示一种物质可转化为另一种物质.“-”表示相连两物质能发生化学反应).其中A、B常温下是气体且组成元素相同,C、D是同类物质,在生产生活中应用广泛.回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 0℃时.甲物质的溶解度为20 | |
| B. | 10℃时.甲.乙两种物质的溶解度相等 | |
| C. | 30℃时.甲物质饱和溶液的质量分数为60% | |
| D. | 除去甲物质中少量乙物质可采取蒸发结晶的方法 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 有机物一定含有碳元素,所以含有碳元素的化合物一定是有机物 | |
| B. | 置换反应有单质生成,则有单质生成的反应一定为置换反应 | |
| C. | 碱溶液显碱性,所以显碱性的溶液一定是碱溶液 | |
| D. | 固体氢氧化钠具有吸水性,所以固体氢氧化钠可用作某些气体的干燥剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
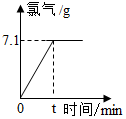 氯化钠是一种重要的化工原料,电解氯化钠溶液可制得氯气、氢氧化钠等物质,发生的化学反应如下:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ Cl2↑+H2↑+2NaOH 现取一定质量的溶质质量分数为10%的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电.生成氯气的质量与反应时间的关系如图所示.请计算:
氯化钠是一种重要的化工原料,电解氯化钠溶液可制得氯气、氢氧化钠等物质,发生的化学反应如下:2NaCl+2H2O $\frac{\underline{\;通电\;}}{\;}$ Cl2↑+H2↑+2NaOH 现取一定质量的溶质质量分数为10%的氯化钠溶液进行电解,当氯化钠完全反应时,停止通电.生成氯气的质量与反应时间的关系如图所示.请计算:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com