
为了测定一份铁镁合金混合粉末中铁的质量分数,某校化学兴趣小组取该样品8g分四次加入盛有100g未知浓度的硫酸溶液的烧杯(已知烧杯质量为50g)中,充分反应后,测得烧杯和烧杯内物质的质量数据记录如下:
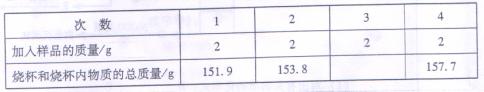
(1)表中第三次加入混合粉末后,烧杯和烧杯内溶液的总质量是 g;
(2)所用硫酸溶液的溶质质量分数是 ;
(3)混合粉末中铁的质量分数是 。
【答案】(1)157.7 (2)14.7% (3)96.25%
【解析】(1)由表格数据可知,每增加2g样品,烧杯内总质量增加1.9g,所以表中第三次加入混合粉末后,烧杯和烧杯内溶液的总质量是153.8g+1.9g=157.7g;
(2)根据质量守恒定律,知反应后烧杯内溶液总质量减少了(100g+50g+8g)-157.7g==0.3g,这就是生成氢气的质量,因为氢气都是来自稀硫酸,所以设稀硫酸中溶质的质量为x,则
H2SO4~H2
98 2
x 0.3g
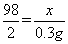 x==14.7g ,
x==14.7g ,
所以所用硫酸溶液的溶质质量分数是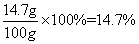 。
。
(3)设混合粉末中铁的质量为y,则混合粉末中镁的质量为8g-y
Fe+H2SO4═FeSO4+H2↑
56 2
y 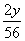
同理:Mg+ H2SO4=MgSO4+H2↑
24 2
8g-y 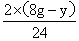
所以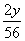 +
+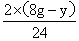 =0.3g
=0.3g
解之得 y=7.7g,混合粉末中铁的质量分数是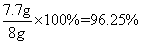 。
。


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:初中化学 来源: 题型:
将4.0g Cu—Zn合金粉末放到盛有10g稀硫酸的烧杯中,恰好完全反应。过滤,称量滤液的质量,相关实验数据如下:
| 反应前物质质量/g | 反应后物质质量/g | |
| Cu—Zn合金 | 稀硫酸 | 滤液质量 |
| 4.0 | 10 | 11.26 |
⑴Cu—Zn合金属于 材料(填“金属”或“有机合成”)。
⑵若不考虑该合金中除Cu、Zn以外的其它成分,请计算原Cu—Zn合金中Zn的质量。写出必要的计算过程。(Zn-65 Cu-63.5 H-1 O-16 S-32)
查看答案和解析>>
科目:初中化学 来源: 题型:
某氢氧化钙中含碳酸钙杂质。称取研细的该样品12.4g放入锥形瓶中,加入32.6g的水,充分振荡形成悬浊液,再向锥形瓶中逐滴滴加盐酸使其充分反应至无气泡产生。测得加入盐酸的质量与锥形瓶中的物质的质量关系如下表示。
| 加入盐酸的质量g | 0 | 25 | 37.5 |
| 锥形瓶中物质的质量 | 45 | 70 | 80.3 |
(1)加入盐酸的质量在0—25g时, 与盐酸发生反应。
(2)反应产生二氧化碳质量为 g。
(3)求样品中氢氧化钙的质量分数(写出计算过程,精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:
二氧化碳是一种宝贵的碳氧资源。以C02和NH3合成尿素CO(NH2)2是固定和利用C02的成功范例,该反该反应的化学方程式为CO2+2NH3=CO(NH2)2,+H20 。请计算:
。请计算:
(1)尿素中C、0、N、H四种元素的质量比(直接写出答案)。
(2)若按上述方法生产120t尿素,可固定的C02的质量为多少。
查看答案和解析>>
科目:初中化学 来源: 题型:
化学实验是进行科学探究的重要方式。
(1)下列实验仪器中不能用于加热的是____(填字母代号)。
a.烧杯 b.量筒 c.试管 d.蒸发皿
(2)某化学小组选用以下装置和药品进行探究实验。
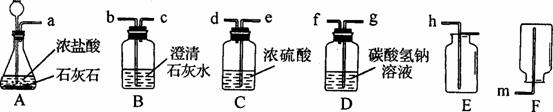 ①A中反应的化学方程式为___________________________________________________。
①A中反应的化学方程式为___________________________________________________。
②若将A、B连接,A中产生的气体并不能使B中的溶液变浑浊,这是为什么?
③若要制取一瓶较为纯净、干燥的CO2,所选用装置的导管接口从左到右的正确连接
顺序为:a接________、_________接________、________接________。
(3)为探究工业废水的综合利用,某化学小组在实验室中完成了以下实验。
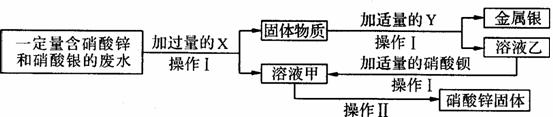 ①X为____;乙与硝酸钡反应的化学方程式为_____________________________________。
①X为____;乙与硝酸钡反应的化学方程式为_____________________________________。
②操作I和操作Ⅱ中都要用到一种玻璃仪器。该仪器在操作Ⅱ中的作用是什么?
(4)某工厂变废为宝,探究用废硫酸等来制取所需产品。现有废硫酸4.9 t(H2SO4的
质量分数为20%),与足量废铁屑反应来制取硫酸亚铁,同时将生成的全部氢气通入足量
氧化铜中并加热(H2+CuO == Cu +H2O),请计算理论上最多可生产铜的质量。
查看答案和解析>>
科目:初中化学 来源: 题型:
某兴趣小组需要配制100g质量分数为9.8%的稀硫酸,假设常温下该稀硫酸的pH值为0,在装有100g该稀硫酸的烧杯中加入104.4gNa2CO3,恰好完全反应,溶液呈中性。
(1)实验室只有98%的浓硫酸,密度为1.84g/cm3,需要量取_____mL(保留一位小数)浓硫酸进行稀释,稀释浓硫酸的方法是_______________________________________
(2)在右图中,画出烧杯内溶液的pH值得变化图像,(标出Na2CO3溶液的质量)
(3)计算所得溶液的溶质质量分数是多少?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
现有20g含Fe2O3为80%的赤铁矿石,加入到150g稀盐酸中,恰好完全反应(铁矿石中杂质都不溶于水,且不与稀盐酸反应)。(计算结果保留一位小数)
求:(1)赤铁矿石中的质量为 g,其中铁元素的质量为 g。
(2)稀盐酸中溶质的质量分数;
(3)恰好完全反应后所得溶液中溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
分类的方法是化学学习中重要的学习方法。下列各组物质按氧化物、混合物、有机物顺序排列的是( )
A.干冰、空气、乙醇
B.生石灰、石油、食盐水
C.水、汽水、纯碱
D.葡萄糖、大理石、纤维素
查看答案和解析>>
科目:初中化学 来源: 题型:
下列关于溶液的说法正确的是( )
A.某温度下两种不同物质的溶液,溶质质量分数相同,则这两种物质的溶解度一定相同
B.溶质质量分数为10%的200毫升某溶液,密度为1.2克/厘米3,其中含溶质24克
C.饱和溶液析出晶体后,溶质的质量分数一定减少
D.不饱和溶液转化为饱和溶液,其溶质的质量分数一定增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com