
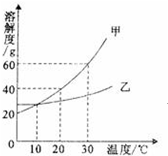
 图中表示的是甲、乙两种固体物质的溶解度曲线,下列叙述一定正确的是( )
图中表示的是甲、乙两种固体物质的溶解度曲线,下列叙述一定正确的是( )分析 根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而甲的溶解度随温度的升高变化比乙大;甲的溶解度大于乙的溶解度不正确,因为没有证明温度;10℃时,甲、乙两物质的溶解度相等正确,因为它们在该温度下有交点;30℃时,甲的溶解度是60g,因此甲的饱和溶液的质量分数=$\frac{60g}{160g}×100%=37.5%$,不是60%.
解答 解:A、甲的溶解度大于乙的溶解度不正确,因为没有证明温度;故选项错误;
B、10℃时,甲、乙两物质的溶解度相等正确,因为它们在该温度下有交点,故选项正确;
C、30℃时,甲的溶解度是60g,因此甲的饱和溶液的质量分数=$\frac{60g}{160g}×100%=37.5%$,不是60%,故选项错误;
D、30℃时,甲的溶解度大于乙的溶解度,故答案为:30℃时,甲的溶解度大于乙的溶解度;
故选B,D中故答案为:30℃时,甲的溶解度大于乙的溶解度;
点评 本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:初中化学 来源: 题型:解答题
| 实验编号 | 1 | 2 |
| 反应物 | 6% H2O2 | 6% H2O2 |
| 催化剂 | 1g红砖粉 | 1g MnO2 |
| 时间 | 152s | 35s |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 因为碱溶液呈碱性,所以呈碱性的溶液一定都是碱溶液 | |
| B. | 不慎将烧碱溶液沾到皮肤上,立即用稀盐酸中和 | |
| C. | 稀释浓硫酸时,将水缓慢倒入浓硫酸中,并不断搅拌 | |
| D. | 中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应 | |
| E. | 用氢氧化钠溶液处理硫在氧气中燃烧产生的气体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com