


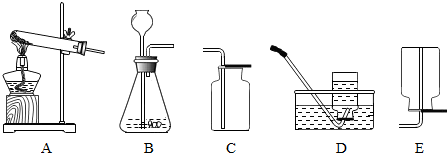
(1)实验室确定气体发生装置时应考虑的因素是_________.
(2)制取氧气时,在装置甲的锥形瓶中放入二氧化锰,在分液漏斗中应加入的是_________,该反应的化学方程式为_________;液体反应物不是一次性加入到锥形瓶中,而是通过分液漏斗逐滴加入,这样做的优点是_________.
(3)制取干燥的氧气时,装置的正确连接顺序是(填导管口的字母)_________.
(4)装置甲也可用来制取二氧化碳,通常可用什么试剂检验所制得的气体是否为二氧化碳?写出检验时所发生反应的化学方程式.
(5)如上图下面的装置也可制取气体,如何检查该装置的气密性?
(6)取12g石灰石(杂质不参加反应)放入锥形瓶中,向其中加入100g一定质量分数的稀盐酸,二者恰好完全反应.反应结束后,锥形瓶中剩余物质的总质量为107.6g.则参加反应的碳酸钙的质量是多少?稀盐酸中溶质的质量分数是多少?
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:阅读理解
 、
、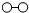 、
、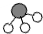 分别表示N2、H2、NH3.在催化剂表面(下图中
分别表示N2、H2、NH3.在催化剂表面(下图中 表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:
表示催化剂表面)N2和H2反应合成氨的反应过程可用五张图表示如下:

查看答案和解析>>
科目:初中化学 来源:学力提升指导丛书 2006年初中化学总复习下册 题型:058
| |||||||||||
查看答案和解析>>
科目:初中化学 来源:2013-2014学年广西省业考试模拟考试化学试卷(解析版) 题型:填空题
人类的生产生活离不开金属材料,随着科技水平的不断提高,金属及其合金在日常生活中扮演着越来越重要的角色。
(1)人们习惯上把金、银、铜、铁、锡五种金属统称为“五金”,在“五金”顺序中把金属 的位置移到最后,正好符合由弱到强的顺序.
(2)汽车车体多用钢材制造。表面喷漆不仅美观,而且可有效防止与 接触而生锈。
(3)工业上用CO还原赤铁矿冶炼金属铁的化学方程为 。
西汉时期中国古老的冶铜方法是“湿法冶铜”主要的反应原理是铁与硫酸铜溶液反应,写出反应的化学方程式
(4)在实验室中探究铝、铜的金属活动性顺序,除铝、铜外,还需要用到的试剂是 。(填一种即可)
(5)铁锅、铝锅是生活中常用的炊具,下图是铁锅的示意图。

①铁锅含有合金单质_______(写化学式),含有的有机合 成材料是_________。(填写名称)
②炒菜时铁锅中的油着火可用锅盖盖灭,其原理是______________________________________。
③铜也易生锈,铜锈的主要成分是碱式碳酸铜(Cu2(OH)2CO3),是铜与空气中的氧气、水和 共同作用的结果.
查看答案和解析>>
科目:初中化学 来源:北京模拟题 题型:实验题


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com